Bland sorterna av okulär allergisk sjukdom har gigantisk papillär konjunktivit (GPC) traditionellt inkluderats vid sidan av säsongsallergier och vernal och atopisk keratokonjunktivit. Vi vet dock dock att GPC inte förtjänar sådan klassificering. Vad vi historiskt sett betraktade som en allergisk reaktion är verkligen resultatet av kronisk irritation i samband med kontaktlinsens kanter, proteser eller suturer. Även om vår kunskap om GPC har utvecklats sedan den först identifierades, dröjer den gamla kategoriseringen.
Förutom denna felaktiga klassificering är GPC också fast med felaktig nomenklatur. GPC är inte riktigt jätte eller papillärt. I vissa fall kallas tillståndet för kontaktlinsinducerad papillär konjunktivit, men många ögonläkare kallar det fortfarande GPC. Och även om det är en konjunktivit, kan det bättre betecknas som en tarsit. En korrekt beskrivning skulle vara miniatyr ojämn övre tarsus.
Här, diskutera väl hur man korrekt diagnostiserar och behandlar detta ofta felaktiga och missförstått tillstånd.
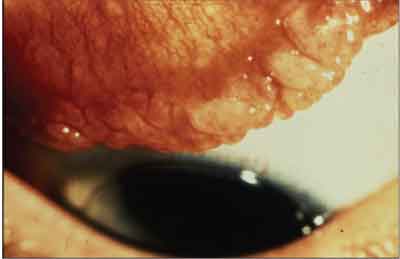
Jätte papillär konjunktivit är inte en allergisk reaktion. Även om det är en konjunktivit, skulle en mer exakt beskrivning vara miniatyr ojämn övre tarsus.
Problemets rot
GPC uppstår när hyperaktivitet hos mastceller och andra immunceller främja kollagentillväxt för att bilda konjunktival papiller.1 Denna tillväxt skiljer papiller i GPC från de som observerats vid bakteriell konjunktivit. Även om denna patofysiologiska mekanism också kan hittas i vårskeratokonjunktivit (VKC), som representerar ett verkligt allergiskt tillstånd, är GPC inte en allergisk reaktion. Vid okulär allergi är nivåerna av histamin, eosinofiler och eosinofilt huvudbasprotein förhöjda; detta är inte fallet med GPC.1
Snarare är GPC ett växande svar på ett kroniskt, fysiskt trauma. Varaktigheten och typen av stimulans som skapar denna mekaniska irritation kan också avgöra presentationen och svårighetsgraden av GPC.
GPC härrör oftast från kontaktlinsförslitning. Roten till problemet är linsens kant, som gnuggar mot ögat när den blinkar 8000 gånger per dag. Detta leder till kronisk irritation som leder till inflammation. GPC: s övervikt hos kontaktlinsbärare tillskrevs ursprungligen en allergi mot linspolymer eller avlagringar, vilket bidrog till att villkoren kategoriserades som en allergi.2
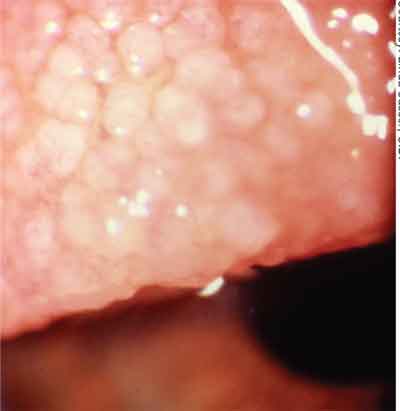
GPC beror på kronisk mekanisk irritation från en kontaktlinskant, skleralspänne eller sutur, vilket orsakar inflammation i tarsal konjunktiva.
Tecken Symtom – De karakteristiska jättepillerna från GPC gör tillståndet lätt identifierbart. Även om sjukdomsnamnet antyder något annat, har papiller av GPC vanligtvis en diameter som inte är större än 0,3 mm; detta är mindre än > 1 mm papiller som ses i VKC. Papiller i GPC inducerad av mjuka linser börjar vanligtvis i den övre zonen av tarsal konjunktiva och utvecklas mot lockets marginal; de har så småningom ett jämnt fördelat mönster över tarsal konjunktiva.
Papiller är inte lika många bland gasgenomsläppliga linsbärare. När de inträffar har de en mer kraterliknande form. Papillernas placering skiljer sig också åt; de som induceras av GP-linser bildas först nära lockets marginal på tarsal konjunktiva.
Uppkomsten av GPC kan inträffa var som helst från några veckor till några år efter initiering av kontaktlinsförslitning och är vanligtvis bilateral, eftersom orsaken (kontaktlinsförslitning) vanligtvis är bilateral. GPC kan vara ensidig om irritationskällan inte är kontaktlinser, utan snarare en abnormitet, såsom en sutur, som också är ensidig.
Ytterligare tecken och symtom på GPC inkluderar sönderrivning, känsla av främmande kroppar, mild till måttlig hyperemi och sträng eller arkliknande slemproduktion. Klåda, ett kännetecken för verkliga allergiska tillstånd, saknas i allmänhet i GPC, och sköldsår eller annat hornhinnans engagemang, typiskt för VKC, förekommer inte i GPC. Att dra i det övre locket tenderar att ge betydande obehag för GPC-patienter på grund av inflammatorisk infiltration i detta område.
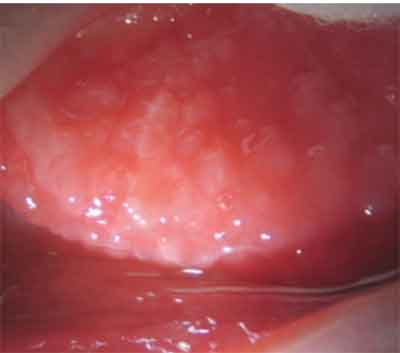
Papiller i GPC är vanligtvis mindre än eller lika till 0,3 mm i diameter och visas på den övre tarsal konjunktiva.
Kan det finnas en koppling mellan dessa individs benägenhet för atopi och deras utveckling av GPC? Motsatsen är förmodligen sant. Brott i den okulära ytbarriären hos GPC-patienter ökar mängden pollen som kan komma igenom mastceller, vilket ökar sannolikheten för att utveckla ögonallergier. Således kan en okulär allergi och GPC uppstå samtidigt hos patienten, vilket komplicerar diagnosen. De två tillstånden kan förvärra varandras tecken och symtom och förvärra det allmänna tillståndet.
Patofysiologi
Den molekylära grunden för GPC börjar med att det normala immunförsvaret störs. Detta stimulerar produktionen och lokaliseringen av inflammatoriska mediatorer, inklusive neutrofiler, eosinofiler och mastceller, i bindhinnan.
Forskning kring medlare som är involverade i GPC har upptäckt fler aktörer i de involverade inflammatoriska processerna. I en nyligen genomförd studie som jämförde cytokin- och kemokinprofiler av VKC och GPC, noterade forskare fyra och åtta gånger ökningen av ett antal inflammatoriska mediatorer i båda sjukdomarna.4 De mest förhöjda i GPC var interleukin-6-löslig receptor (IL-6sR), interleukin-11 (IL-11), eotaxin-2, makrofaginflammatoriskt protein (MIP) -1 delta och vävnadshämmare av metalloproteinas-2 (TIMP-2), även om endast TIMP-2 och IL-6sR ökningar var signifikanta jämfört med kontroller. Även om några av samma medlare var förhöjda i både GPC och VKC, var TIMP-2 den enda medlare som utvärderades i denna studie som var signifikant förhöjd hos GPC-patienter jämfört med dem som hade VKC. IL-6sR var signifikant förhöjt i både VKC och GPC. Detta, tillsammans med ökningen av andra cytokiner, deras receptorer och kemokiner, betonar vikten av dessa medlare för patofysiologin hos båda tillstånden.
Annan forskning har utvärderat T-cellprofilerna i GPC och kroniska former av allergi för att avgöra vilka andra inflammatoriska mekanismer förutom typ I överkänslighet är på jobbet. Förskjutningen mot övervägande Th2-cytokiner var mer uttalad i GPC och VKC, medan atopisk keratokonjunktivit (AKC) avslöjade en mer Th1-liknande cytokinprofil.5 Forskare säger att dessa skillnader kan hjälpa till att förklara de kliniska manifestationerna av dessa tillstånd och kan påverka terapeutiska beslut. .
Ytterligare forskning avslöjade att de inflammatoriska markörerna humant leukocytantigen (HLA) -DR och intercellulär vidhäftningsmolekyl (ICAM) -1 var högre än normalt i GPC, även om ökningarna var mindre än de som sågs i AKC och VKC.6 Höjningen av ICAM-1 indikerar sannolikt rekrytering av leukocyter av epitelceller.
Forskare undersökte också en rad cytokiner för deras närvaro eller förhöjning i VKC, AKC och GPC. Några skillnader hittades, såsom uppreglering av cytokinet RANTES (Reglerat på aktivering, Normal T uttryckt och utsöndrat) i GPC men inte i AKC och VKC.6 Variabiliteten i cytokinprofil med varje sjukdom kan ge potentiella mål för framtida terapier inriktade vid varje specifikt tillstånd.
Forskare avslöjade också att underliggande hornhinnans involvering av VKC och AKC är ett större uttryck för eosinofila ytantigener än vad som ses med GPC såväl som skillnader i vilka cytokiner var framträdande, jämfört med GPC.7. av proteinet eotaxin i GPC har fått ett visst intresse, men detta är fortfarande diskutabelt. Viss forskning visar förhöjt eotaxin i tårarna hos kontaktlinsbärare och en korrelation mellan svårighetsgraden av tecken på GPC med eotaxinnivåer.8 Ytterligare en annan studie, som utvärderade 68 fall av GPC på grund av ögonproteser, fann inga signifikanta skillnader i tåren eotaxinnivåerna hos dessa individer jämfört med friska försökspersoner.9 Eotaxinnivåerna minskade faktiskt vid kronisk GPC. Ytterligare forskning kan fastställa om olika etiologier av GPC faktiskt resulterar i särskiljbara skillnader i profilen för inflammatoriska mediatorer som uttrycks eller om den temporala utvecklingen av GPC från akut till kronisk förändrar eotaxinnivåerna.
Behandling
Forskning som undersöker medlare och patogenes av GPC, liksom jämförelser av dess likheter och skillnader mot kroniska allergier, fortsätter. Denna forskning har potential för utveckling av framtida terapier.
Hantering av GPC idag är dock bäst inriktad på förebyggande. Att identifiera och ta bort orsaken är viktigt för att lösa tillståndet. Upprätthålla konstant vakenhet för GPC hos bärare av kontaktlinser. I linsinducerad GPC är mjuka kontaktlinser oftare inblandade än hårda linser.10
Kom ihåg att linsens kant är nyckelkomponenten för förebyggande. Vi och andra har sett fall där samma linspolymer används i båda ögonen, men var och en har en annan linskant, vilket leder till utveckling av GPC endast i det högre myopiska ögat. Sådana fall exemplifierar sambandet mellan GPC och linskant eftersom alla andra variabler kontrolleras.
Dessutom får ingen avvisa korrekt linsvårdshygien och bärvanor. Studier har visat att frekvensen för linsbyte är nära korrelerad med förekomsten av GPC. En studie som utvärderade 47 kontaktlinsbärare fann att GPC inträffade hos 36% av patienter vars linsersättningsschema översteg fyra veckor jämfört med 4,5% av dem som bytte lins oftare än en gång var fjärde vecka.11 Medan ett tätare schema för linsbyte inte kan eliminera risken för GPC, visar resultaten av denna studie att detta mönster av linsbyte kan minimera risken.
Tidig identifiering och avlägsnande av den orsakande faktorn är det snabbaste sättet att lösa GPC. Om kontaktlinser är orsaken är det vanligt att avlägsnande under en till tre veckor är tillräckligt för att symtomen ska avta, även om papiller kan dröja kvar i flera månader. När kontaktlinsförslitningen återupptas, överför patienten till en annan typ av lins för att försöka hitta en linskantdesign som är mindre irriterande för den individen snarare än att återinföra samma lins som användes vid tidpunkten för GPC-identifiering.
Steroider som loteprednoletabonat kan användas för att behandla inflammation i samband med allvarligare fall av GPC. Detta tar dock inte upp den bakomliggande orsaken till GPC, så deras användning bör åtföljas samtidigt av ett linsslitage och de ska inte användas på lång sikt. Mastcellstabilisatorer kan också ordineras; emellertid, eftersom mekanismen för GPC inte primärt är en mastcellmedierad process som säsongsbunden allergisk konjunktivit är, har dessa begränsad effekt.
Genom att förstå att jätte papillär konjunktivit inte är en allergi utan ett inflammatoriskt tillstånd som härrör från upprepad mekanisk irritation (troligen över kontaktlinsens kant) kan vi bättre identifiera och behandla dessa patienter. Och GPC-dagarna som maskerar sig som en sann allergi är snart över.
Dr. Chin är biträdande professor i optometri vid New England College of Optometry i Boston. Han praktiserar vid Andover Eye Associates, Andover, Mass., Och utför klinisk forskning vid Ophthalmic Research Associates, North Andover, Mass.
1. Greiner JV. Jätte papillär konjunktivit. I: Allergiska sjukdomar i ögat. Abelson MB, red. New York: WB Saunders; 2001: 140-60.
3. Begley CG, Riggle A, Tuel JA. Förening av jätte papillär konjunktivit med säsongsallergier. Optom Vis Sci 1990; 67: 192.
4. Shoji J, Inada N, Sawa M.Antikroppsgenererade cytokinprofiler av tårar hos patienter med vernal keratokonjunktivit eller jätte papillär konjunktivit. Jpn J Ophthalmol 2006 maj-juni; 50 (3): 195-204.
6. Hingorani M, Calder VL, Buckley RJ, Lightman SL. Rollen av konjunktival epitelceller i kronisk okulär allergisk sjukdom. Exp Eye Res 1998 nov; 67 (5): 491-500.
7. Hingorani M, Calder V, Jolly G, et al. Eosinofilt ytantigenuttryck och cytokinproduktion varierar i olika okulära allergiska sjukdomar. J Allergy Clin Immunol 1998 nov; 102 (5): 821-30.
9. Sarac O, Erdener U, Irkec M, et al. Riv eotaxinnivåerna i jätte papillär konjunktivit associerad med ögonproteser. Ocul Immunol Inflamm 2003 Sep; 11 (3): 223-30.
10. Donshik PC. Jätte papillär konjunktivit. Trans Am Ophthalmol Soc 1994; 92: 687-744.
11. Donshik PC, Porazinski AD. Jätte papillär konjunktivit hos frekventa ersättningskontaktlinsbärare: en retrospektiv studie Trans Am Ophthalmol Soc 1999; 97: 205-16.