O gelo flutua porque é menos denso que a água. A água tem uma densidade de 1,0 gm / cm cúbico.
A densidade do gelo Ih é 0,931 gm / cm cúbico.
Mas, por que o gelo é menos denso do que a água se ambos são feitos acima de moléculas de H2O?
————– > gire em ——– > – spin off
—— > preenchimento de espaço / cpk ——– > vara —- > bola e vara
Para girar a molécula — > Clique com o botão esquerdo e arraste
para ampliar – > > Clique com o botão esquerdo + mantenha pressionada a tecla Shift botão e arraste verticalmente
Menu Jsmol — > > Clique com o botão direito
Experimente !!
Mude para wireframe primeiro:
Clique com o botão direito do mouse sobre a caixa
Estilo – > Esquemas – – > wireframe
Rótulo de átomos:
Estilo – > Rótulo — > número do átomo
Meça os seguintes ângulos:
< 415
< 512
< 213
< 314
Para medir ângulos: segure a parte inferior esquerda do mouse sobre o átomo e clique duas vezes no átomo 1, arraste para o segundo átomo (átomo central) clique uma vez no átomo central, arraste e clique duas vezes no átomo 3.
—— > preenchimento de espaço / cpk ——– > stick —- > ball-and-stick
A água líquida tem uma estrutura parcialmente ordenada na qual ligações de hidrogênio estão constantemente sendo formadas e quebrando.
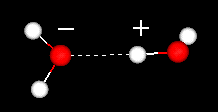
Por outro lado, o gelo tem uma estrutura de rede rígida.
Na água líquida, cada molécula é ligada por hidrogênio a aproximadamente 3,4 outras moléculas de água.
No gelo, cada molécula é ligada por hidrogênio a 4 outras moléculas.
Compare as duas estruturas abaixo. Observe os espaços vazios na estrutura de gelo.
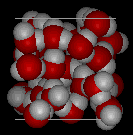 |
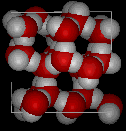 |
No gelo Ih, cada água se forma quatro ligações de hidrogênio com distâncias O — O de 2,76 Angstroms até o vizinho de oxigênio mais próximo. Por causa da estrutura ordenada no gelo, há menos moléculas de H20 em um determinado espaço de volume.
Tente isto –
Tente isto –
1) Meça as distâncias OO entre quaisquer dois átomos de oxigênio adjacentes no gelo mostrado na estrutura acima.
Por favor, digite sua resposta no espaço fornecido:
Ao contrário do gelo – a água em temperatura ambiente está em movimento constante – as ligações de hidrogênio são formadas e quebradas constantemente – clique aqui para ver as moléculas de água em movimento