Entre as variedades de doença alérgica ocular, a conjuntivite papilar gigante (GPC) tem sido tradicionalmente incluída ao lado de alergias sazonais e ceratoconjuntivite vernal e atópica. Agora sabemos, entretanto, que o GPC não merece tal classificação. O que historicamente consideramos uma reação alérgica, na verdade, é o resultado de irritação crônica associada a bordas de lentes de contato, próteses ou suturas. Embora nosso conhecimento do GPC tenha avançado desde que foi identificado pela primeira vez, a velha categorização perdura.
Além dessa classificação incorreta, o GPC também está preso a uma nomenclatura incorreta. GPC não é verdadeiramente gigante nem papilar. Em alguns casos, a condição é conhecida como conjuntivite papilar induzida por lentes de contato, mas muitos oftalmologistas ainda a chamam de GPC. E, embora seja uma conjuntivite, pode ser melhor designada como tarsite. Uma descrição precisa seria o tarso superior em miniatura irregular.
Aqui, discutiremos como diagnosticar e tratar corretamente essa condição frequentemente mal identificada e mal compreendida.
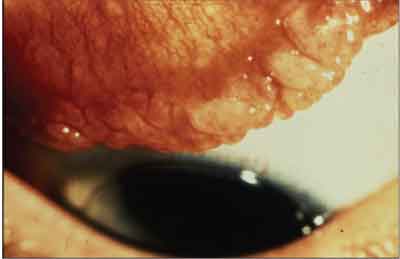
A conjuntivite papilar gigante não é uma reação alérgica. Embora seja uma conjuntivite, uma descrição mais precisa seria o tarso superior irregular em miniatura.
A raiz do problema
GPC ocorre quando a hiperatividade dos mastócitos e outras células do sistema imunológico promovem o crescimento do colágeno para formar papilas conjuntivais.1 Esse crescimento distingue as papilas em GPC daquelas observadas na conjuntivite bacteriana. Embora esse mecanismo fisiopatológico também possa ser encontrado na ceratoconjuntivite primaveril (VKC), que representa uma condição alérgica verdadeira, a GPC não é uma reação alérgica. Na alergia ocular, os níveis de histamina, eosinófilos e proteína básica principal eosinofílica estão elevados; este não é o caso com GPC.1
Em vez disso, GPC é uma resposta proliferada a um trauma físico crônico. A duração e o tipo de estímulo que cria essa irritação mecânica também podem determinar a apresentação e a gravidade do GPC.
O GPC geralmente se origina do uso de lentes de contato. A raiz do problema é a borda da lente, que esfrega contra o olho enquanto pisca 8.000 vezes por dia. Isso leva à irritação crônica que resulta em inflamação. A preponderância de GPC em usuários de lentes de contato foi originalmente atribuída a uma alergia a polímeros ou depósitos de lentes, contribuindo para a classificação incorreta das condições como uma alergia.2
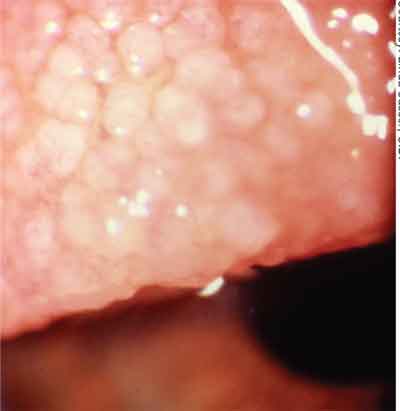
GPC resulta de irritação mecânica crônica de uma borda de lente de contato, fivela escleral ou sutura, que causa inflamação da conjuntiva tarsal.
Sinais e Sintomas
As papilas gigantes características da GPC tornam a condição prontamente identificável. Embora o nome da doença implique o contrário, as papilas de GPC normalmente têm um diâmetro não maior que 0,3 mm; isso é menor do que as > papilas de 1 mm vistas no VKC. As papilas em GPC induzidas por lentes moles normalmente começam na zona superior da conjuntiva tarsal e progridem em direção à margem palpebral; eventualmente, apresentam um padrão uniformemente disperso pela conjuntiva tarsal.
As papilas não são tão numerosas em usuários de lentes permeáveis a gás. Quando ocorrem, têm uma forma mais parecida com uma cratera. A localização das papilas também difere; aqueles induzidos por lentes GP formam-se primeiro perto da margem da pálpebra da conjuntiva tarsal.
O início da GPC pode ocorrer em qualquer lugar de algumas semanas a alguns anos após o início do uso de lentes de contato e é tipicamente bilateral, pois a causa (uso de lentes de contato) é tipicamente bilateral. O GPC pode ser unilateral se a fonte da irritação não forem lentes de contato, mas sim uma anormalidade, como uma sutura, que também é unilateral. Sinais e sintomas adicionais de GPC incluem lacrimejamento, sensação de corpo estranho, hiperemia leve a moderada e produção de muco viscoso ou em forma de folha. O prurido, uma característica marcante das verdadeiras condições alérgicas, geralmente está ausente no GPC, e as úlceras em escudo ou outro envolvimento da córnea, típico de VKC, não ocorrem no GPC. Puxar a pálpebra superior tende a produzir desconforto significativo para pacientes com GPC devido ao infiltrado inflamatório nessa área.
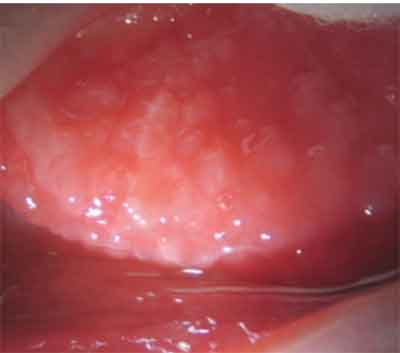
As papilas no GPC são geralmente menores ou iguais até 0,3 mm de diâmetro e aparecem na conjuntiva tarsal superior.
Poderia haver associação entre a predisposição desses indivíduos à atopia e o desenvolvimento de GPC? O oposto provavelmente é verdade. Rupturas na barreira da superfície ocular de pacientes com GPC aumentam a quantidade de pólen que pode chegar aos mastócitos, o que aumenta a probabilidade de desenvolver alergias oculares. Assim, uma alergia ocular e GPC podem ocorrer simultaneamente no paciente, dificultando o diagnóstico. As duas condições podem exacerbar os sinais e sintomas da outra, piorando a condição geral.
Fisiopatologia
A base molecular da GPC começa com a interrupção das defesas imunológicas normais. Isso estimula a produção e localização de mediadores inflamatórios, incluindo neutrófilos, eosinófilos e mastócitos, na conjuntiva.
A pesquisa sobre os mediadores envolvidos na GPC revelou mais participantes nos processos inflamatórios envolvidos. Em um estudo recente que comparou os perfis de citocinas e quimiocinas de VKC e GPC, os pesquisadores observaram aumentos de quatro e oito vezes em numerosos mediadores inflamatórios em ambas as doenças, respectivamente.4 Os mais elevados em GPC foram o receptor solúvel de interleucina-6 (IL-6sR), interleucina-11 (IL-11), eotaxina-2, proteína inflamatória de macrófagos (MIP) -1 delta e inibidor tecidual de metaloproteinase-2 (TIMP-2), embora apenas aumentos de TIMP-2 e IL-6sR tenham sido significativos quando comparados com controles. Embora alguns dos mesmos mediadores estivessem elevados em ambos GPC e VKC, o TIMP-2 foi o único mediador avaliado neste estudo que estava significativamente elevado em indivíduos com GPC em comparação com aqueles que tinham VKC. IL-6sR foi significativamente elevado em ambos VKC e GPC. Isso, juntamente com o aumento de outras citocinas, seus receptores e quimiocinas, enfatiza a importância desses mediadores para a fisiopatologia de ambas as condições.
Outra pesquisa avaliou os perfis de células T no GPC e nas formas crônicas de alergia para determinar quais outros mecanismos inflamatórios além da hipersensibilidade do tipo I estão em ação. A mudança para citocinas predominantemente Th2 foi mais pronunciada em GPC e VKC, enquanto a ceratoconjuntivite atópica (AKC) revelou um perfil de citocinas mais Th1-like.5 Os pesquisadores dizem que essas diferenças podem ajudar a explicar as manifestações clínicas dessas condições e podem influenciar as decisões terapêuticas .
Outras pesquisas revelaram que os marcadores inflamatórios antígeno leucocitário humano (HLA) -DR e molécula de adesão intercelular (ICAM) -1 foram elevados acima do normal em GPC, embora os aumentos tenham sido menores do que aqueles observados em AKC e VKC.6 A elevação de ICAM-1 provavelmente indica o recrutamento de leucócitos por células epiteliais. Os pesquisadores também examinaram uma série de citocinas quanto à sua presença ou elevação em VKC, AKC e GPC. Algumas diferenças foram encontradas, como a suprarregulação da citocina RANTES (Regulada na Ativação, Normal T Expressada e Secreta) em GPC, mas não em AKC e VKC.6 A variabilidade no perfil de citocinas com cada doença pode apresentar alvos potenciais para futuras terapias visadas em cada condição específica.
Os pesquisadores também revelaram que subjacente ao envolvimento corneano de VKC e AKC está uma maior expressão de antígenos de superfície de eosinófilos do que é observada com GPC, bem como diferenças nas quais as citocinas eram proeminentes, em comparação com GPC.7
O possível envolvimento da proteína eotaxina em GPC ganhou algum interesse, mas isso permanece discutível. Algumas pesquisas mostram eotaxina elevada nas lacerações de usuários de lentes de contato e uma correlação entre a gravidade dos sinais de GPC com os níveis de eotaxina.8 Ainda outro estudo, que avaliou 68 casos de GPC devido a próteses oculares, não encontrou diferenças significativas na ruptura os níveis de eotaxina nesses indivíduos em comparação com indivíduos saudáveis.9 Na verdade, os níveis de eotaxina diminuíram no GPC crônico. Pesquisas adicionais podem estabelecer se as diferentes etiologias de GPC realmente resultam em diferenças distinguíveis no perfil de mediadores inflamatórios expressos ou se a progressão temporal de GPC de aguda para crônica altera os níveis de eotaxina.
Tratamento
Pesquisa que investiga os mediadores e patogênese de O GPC, bem como as comparações de suas semelhanças e diferenças com as alergias crônicas, continua. Esta pesquisa tem potencial para o desenvolvimento de terapias futuras. O gerenciamento de GPC hoje, entretanto, é mais focado na prevenção. Identificar e remover a causa é essencial para resolver a condição. Mantenha alerta constante para GPC em usuários de lentes de contato. No GPC induzido por lentes, as lentes de contato gelatinosas estão mais frequentemente envolvidas do que as lentes rígidas.10
Lembre-se de que a borda da lente é o principal componente da prevenção. Nós e outros vimos casos em que o mesmo polímero de lente é usado em ambos os olhos, mas cada um tem uma borda de lente diferente, levando ao desenvolvimento de GPC apenas no olho com miopia superior. Tais casos exemplificam a associação entre GPC e borda da lente porque todas as outras variáveis são controladas.Além disso, ninguém deve descartar os hábitos adequados de uso e higiene dos cuidados com as lentes. Estudos demonstraram que a frequência de substituição das lentes está intimamente relacionada à incidência de GPC. Um estudo que avaliou 47 usuários de lentes de contato descobriu que GPC ocorreu em 36% dos indivíduos cujos cronogramas de troca de lentes excederam quatro semanas versus 4,5% daqueles que trocaram de lentes com mais frequência do que uma vez a cada quatro semanas.11 Embora um cronograma de troca de lentes mais frequente não possa inteiramente eliminar o risco de GPC, os resultados deste estudo indicam que este padrão de substituição de lentes pode minimizar esse risco.
A identificação precoce e remoção do fator causal são os meios mais rápidos para resolver GPC. Se as lentes de contato forem a causa, a remoção por uma a três semanas geralmente é suficiente para que os sintomas diminuam, embora as papilas possam durar meses. Quando o uso das lentes de contato retomar, faça a transição do paciente para um tipo diferente de lente para tentar encontrar um design de borda de lente que seja menos irritante para aquele indivíduo, em vez de reintroduzir a mesma lente usada no momento da identificação de GPC.
Esteróides como o etabonato de loteprednol podem ser usados para tratar a inflamação associada a casos mais graves de GPC. No entanto, isso não aborda a causa subjacente do GPC, portanto, seu uso deve ser acompanhado simultaneamente por um intervalo de uso da lente e não deve ser usado por um longo prazo. Estabilizadores de mastócitos também podem ser prescritos; no entanto, como o mecanismo de GPC não é principalmente um processo mediado por mastócitos como a conjuntivite alérgica sazonal, esses são de eficácia limitada.
Compreendendo que a conjuntivite papilar gigante não é uma alergia, mas uma condição inflamatória que resulta de irritações mecânicas repetidas (provavelmente na borda da lente de contato), podemos identificar e tratar melhor esses pacientes. E os dias de GPC disfarçados de uma alergia verdadeira logo acabarão.
Dr. Chin é professor assistente de optometria no New England College of Optometry em Boston. Ele atende na Andover Eye Associates, Andover, Mass., E realiza pesquisas clínicas na Ophthalmic Research Associates, North Andover, Mass.
1. Greiner JV. Conjuntivite papilar gigante. In: Doenças alérgicas do olho. Abelson MB, ed. Nova York: WB Saunders; 2001: 140-60.
3. Begley CG, Riggle A, Tuel JA. Associação de conjuntivite papilar gigante com alergias sazonais. Optom Vis Sci 1990; 67: 192.
4. Shoji J, Inada N, Sawa M. Perfis de citocinas geradas por matriz de anticorpos de lágrimas de pacientes com ceratoconjuntivite primaveril ou conjuntivite papilar gigante. Jpn J Ophthalmol maio-junho de 2006; 50 (3): 195-204.
6. Hingorani M, Calder VL, Buckley RJ, Lightman SL. O papel das células epiteliais conjuntivais na doença alérgica ocular crônica. Exp Eye Res, novembro de 1998; 67 (5): 491-500.
7. Hingorani M, Calder V, Jolly G, et al. A expressão do antígeno de superfície de eosinófilos e a produção de citocinas variam em diferentes doenças alérgicas oculares. J Allergy Clin Immunol, novembro de 1998; 102 (5): 821-30.
9. Sarac O, Erdener U, Irkec M, et al. Níveis de rasgo de eotaxina na conjuntivite papilar gigante associada a próteses oculares. Ocul Immunol Inflamm Set 2003; 11 (3): 223-30.
10. Donshik PC. Conjuntivite papilar gigante. Trans Am Ophthalmol Soc 1994; 92: 687-744.
11. Donshik PC, Porazinski AD. Conjuntivite papilar gigante em usuários de lentes de contato de substituição frequente: um estudo retrospectivo. Trans Am Ophthalmol Soc 1999; 97: 205-16.