O termo condução aberrante refere-se ao bloqueio transitório do ramo não devido a anormalidades QRS anteriores, condução da via acessória ou efeitos indesejados de drogas. 1 O bloqueio pode ocorrer em qualquer nível do sistema His-Purkinje e pode ser devido a diferentes mecanismos. O bloqueio de fase 3 (dependente de taquicardia) é devido à invasão de tecido durante o período refratário efetivo e pode ser um fenômeno fisiológico ou patológico. Uma forma especial desse bloqueio é o bloqueio dependente da aceleração, que se deve a alterações na freqüência cardíaca. O bloqueio de fase 4 (dependente de bradicardia ou dependente de pausa) é quase sempre patológico. Ocorre após o término do período refratário por diminuição do potencial de membrana, aumento da automaticidade de His-Purkinje ou despolarização parcial da lesão miocárdica. O quarto e último mecanismo aberrante é devido à condução oculta, que é definida como a propagação de um impulso dentro do sistema de condução específico e só pode ser reconhecido por seu efeito no impulso, no intervalo ou nos ciclos seguintes.2 Conforme indicado por seu nome, esse fenômeno não pode ser observado no eletrocardiograma de superfície (ECG).
Apresentamos o caso de uma mulher de 86 anos que deu entrada no serviço de emergência por palpitações e dispneia. Alguns anos antes, ela havia sido avaliada por um cardiologista por bradicardia sinusal assintomática, para a qual não estava recebendo tratamento. O exame físico revelou bulhas cardíacas irregulares de baixa intensidade sem sopros e estertores bibasais sem outros achados de interesse. Na admissão, o ECG apresentava fibrilação atrial com resposta ventricular em torno de 100 bpm, com bloqueio fascicular anterior esquerdo (LAFB), alternando com batimentos com complexo QRS mais estreito (Figura 1A e Figura no material suplementar). Durante a internação no pronto-socorro, a paciente recebeu 2,5 mg de atenolol por via venosa e atingiu ritmo sinusal a uma taxa de 39 bpm, com normalização da morfologia do QRS (Figura 1B e Figura no material complementar). O paciente recebeu alta sem medicação antiarrítmica. Às 3 semanas, ela foi internada com astenia acentuada e bradicardia sinusal documentada a 35 bpm, para a qual recebeu um marcapasso DDD.
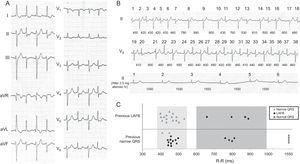
A: Eletrocardiógrafo de 12 derivações. B: Traçado de ECG completo na admissão. Os batimentos 1–38 são consecutivos, apesar de estarem em 2 derivações diferentes (II e V5). As durações dos ciclos entre as batidas são mostradas em milissegundos. O painel inferior mostra a morfologia QRS após a administração intravenosa de 2,5 mg de atenolol e conversão para ritmo sinusal. C: A relação da morfologia QRS com a duração do ciclo e a morfologia do batimento anterior. LAFB, bloqueio fascicular anterior esquerdo.
A análise cuidadosa do ECG obtido durante o episódio mostrou claramente 2 tipos de QRS: a) QRS com morfologia LAFB (120ms), alternando com b) QRS estreito com pequeno variações no eixo e duração (90-100ms). Além disso, em intervalos R – R mais longos, os batimentos sempre tiveram morfologia LAFB. Duas áreas podem ser claramente diferenciadas na Figura 1C, que compara a morfologia do QRS com a duração do ciclo e o complexo QRS anterior.3 Na zona 1 (R – R, 400–530 ms), a morfologia do QRS depende do batimento anterior , (ou seja, se o batimento anterior for estreito, o batimento seguinte terá morfologia LAFB). As únicas exceções a esta regra são os batimentos 32-33, que podem ser explicados pela penetração do impulso na fase de condução sobrenatural do fascículo anterior.3,4 No entanto, na zona 2 (R – R 600ms), o complexo QRS sempre tem morfologia LAFB independentemente da morfologia do batimento anterior, o que é sugestivo de bloqueio dependente de bradicardia. O curioso desse caso é que, ao contrário do que seria esperado neste tipo de bloqueio, após um intervalo RR muito maior (> 1500ms), o QRS torna-se normal.
A Figura 2 mostra o mecanismo proposto para essas descobertas. Com intervalos R – R curtos (zona 1), um bloqueio anterógrado e retrógrado ocorre no fascículo anterior, o que torna o impulso seguinte capaz de conduzir anterógradamente desde que haja tempo de repolarização. Desse modo, as pequenas variações nos complexos QRS estreitos poderiam ser explicadas por ocorrerem em diferentes momentos de seu período refratário relativo, com maior ou menor grau de latência (por exemplo, batimentos 3 e 7, ou 13 e 15). Com ciclos muito longos, ocorre a recuperação do tecido e a condução anterógrada permanente. Cohen e cols.5 descreveram esse fenômeno no final da década de 1970 e o chamaram de bloqueio alternativo de ramo dependente de pseudobradicardia (ou seja, bloqueio de fase 3).Para que isso ocorra, o período refratário efetivo retrógrado do fascículo anterior deve ser menor do que o período refratário efetivo anterógrado e, assim, favorecer a condução retrógrada oculta. = “28de12520e”>
A. Mecanismo proposto dos achados eletrocardiográficos. As barras pretas representam os períodos refratários efetivos teóricos e as linhas pontilhadas oblíquas representam a condução interfascicular retrógrada oculta. B. Confirmação do mecanismo com estimulação atrial (AAI). AF, fascículo anterior; CL, duração do ciclo; PF, fascículo posterior; RB, ramificação direita.
Conseguimos confirmar esse mecanismo (Figura 2B) porque nosso paciente havia recebido um marca-passo DDD implantado. LAFB alternado foi produzido por estimulação AAI a 100 bpm, a 70 bpm todos os batimentos foram conduzidos com morfologia LAFB e a 60 bpm todos os batimentos foram estreitos, o que confirmou o bloqueio dependente de taquicardia.