Personne naime lidée de vieillir. Malgré nos nombreux efforts humains pour échapper ou retarder le processus de vieillissement, cela semble être une partie inévitable de la vie.
Mais… pourquoi? Pourquoi les êtres vivants se désagrègent-ils progressivement en vieillissant?
Il y a un mot pour cela: la sénescence. Non, ce n’est pas le groupe de rock qui a chanté « Bring Me to Life »; la sénescence est létat de détérioration progressive du fonctionnement normal. Au niveau cellulaire, cela signifie que les cellules arrêtent de se diviser et finissent par mourir. Cela peut également sappliquer à un organisme entier (où un être vivant ne peut plus répondre adéquatement aux facteurs de stress extérieurs), ou à des organes ou tissus spécifiques (comme les feuilles qui meurent et tombent des arbres en automne).
sont des moyens par lesquels nous pouvons ralentir (ou accélérer) la vitesse à laquelle la sénescence se produit, cela va encore se produire dune manière ou dune autre. Cependant, quelques espèces peuvent échapper complètement au processus de vieillissement.
La méduse «immortelle», Turritopsis dohrnii
À ce jour, il ny a quune seule espèce qui a été appelée «biologiquement immortelle»: la méduse Turritopsis dohrnii. Ces petits animaux transparents traînent dans les océans du monde entier et peuvent remonter le temps en revenant à une étape antérieure de leur cycle de vie.
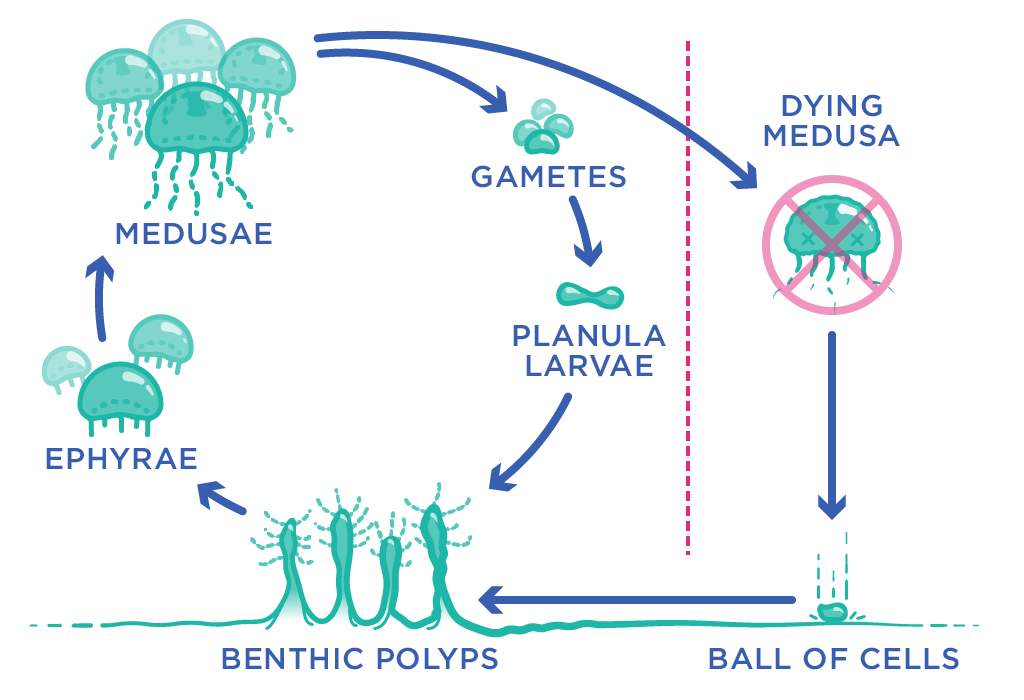
Une nouvelle vie de méduse commence avec un œuf fécondé, qui se transforme en un stade larvaire appelé planula. Après une nage rapide, la planule se verrouille sur une surface (comme un rocher, ou le fond de locéan, ou la coque dun bateau), où elle se développe en un polype: une structure en forme de tube avec une bouche à une extrémité et une sorte de pied à lautre. Il reste bloqué en place pendant un certain temps, devenant une petite colonie de polypes qui partagent des sondes dalimentation les uns avec les autres.
Finalement, selon lespèce de méduse, lun de ces polypes formera une excroissance appelée bud , ou il peut produire des segments séparés empilés les uns sur les autres, qui peuvent alors se détacher du reste de la colonie. Ce processus est responsable des étapes suivantes du cycle de vie des méduses: léphyre (une petite méduse) et la méduse, qui est le stade adulte entièrement formé capable de reproduction sexuée.
Pour la plupart des autres méduses, cette étape est la fin de la ligne. Mais Turritopsis dohrnii (et peut-être dautres espèces de méduses aussi) a une astuce de fête: quand il est confronté à une sorte de stress environnemental, comme la famine ou une blessure, il peut redevenir une petite goutte de tissu, qui se transforme ensuite en phase polype sexuellement immature de la vie. Cest un peu comme un papillon redevenant chenille, ou une grenouille redevenant un têtard.
Bien sûr, Turritopsis dohrnii nest pas vraiment «immortel». Ils peuvent encore être consommés par les prédateurs ou tués par dautres moyens. Cependant, leur capacité à basculer entre les étapes de la vie en réponse au stress signifie quen théorie, ils pourraient vivre éternellement.
Hydra
Lhydre ressemble un peu au polype stade dune méduse (ce qui a du sens, étant donné que la méduse et lhydre sont regroupées dans le phylum Cnidaria): un corps tubulaire avec une bouche aux tentacules à une extrémité et un pied adhésif à lautre. Ce sont des animaux très simples qui passent la plupart de leurs journées à rester au même endroit dans des étangs deau douce ou des rivières et à utiliser leurs tentacules piquants pour attraper toute proie qui passe à la nage.

Leur prétention à limmortalité? Il semble qu’ils ne passent pas du tout par la sénescence. Au lieu de se détériorer progressivement avec le temps, les cellules souches d’une hydre ont la capacité d’un auto-renouvellement infini. Cela semble être dû à un ensemble particulier de gènes appelés gènes FoxO, qui se trouvent chez les animaux, des vers aux humains, et jouent un rôle dans la régulation de la durée de vie des cellules.
Dans le cas de la tige dHydra cellules, il semble y avoir une surabondance dexpression du gène FoxO. Lorsque les chercheurs ont empêché les gènes FoxO de fonctionner, ils ont découvert que les cellules dHydra commençaient à montrer des signes de vieillissement et ne se régénéraient plus comme avant. Nous ne savons toujours pas exactement comment tout cela fonctionne, mais nous savons que ces gènes jouent clairement un rôle important dans le maintien de la jeunesse infinie dHydra.
Des homards pas tout à fait immortels
Les homards ne subissent pas non plus de sénescence. Contrairement à la dépendance dHydra sur des gènes particuliers, cependant, leur longévité est due à leur capacité à réparer sans fin leur ADN.
Normalement, pendant le processus de copie dADN et de division cellulaire, les capuchons protecteurs sur les chromosomes, appelés télomères, deviennent lentement de plus en plus courts, et quand ils sont trop courts, une cellule entre en sénescence et ne peut pas continuez à diviser.

Les homards nont pas ce problème grâce à un approvisionnement sans fin dune enzyme appelée télomérase, qui fonctionne pour continuer à régénérer les télomères. Ils produisent beaucoup de cette enzyme dans toutes leurs cellules tout au long de leur vie adulte, ce qui leur permet de maintenir indéfiniment un ADN juvénile.
La télomérase nest pas unique aux homards. Il est présent chez la plupart des autres animaux, y compris les humains, mais après avoir dépassé le stade de la vie embryonnaire, les niveaux de télomérase dans la plupart des autres cellules diminuent et ne sont pas suffisants pour reconstruire constamment les télomères.
Malheureusement pour les homards, cependant, il y a un hic: ils deviennent littéralement trop gros pour leurs propres coquilles. Les homards grandissent continuellement de plus en plus gros, mais leurs coquilles ne peuvent pas changer de taille, ce qui signifie toute une vie dabandonner des coquilles trop petites et de cultiver un tout nouvel exosquelette à chaque fois. Cela demande beaucoup dénergie. Finalement, la quantité dénergie requise pour muer une coquille et en faire pousser une autre est tout simplement trop élevée. Le homard succombe à lépuisement, à la maladie, à la prédation ou à leffondrement de sa coquille.
Toujours jeune?
Il existe de nombreuses autres espèces animales (et non animales!) Qui offrent des aperçus alléchants dans un âge sans âge existence: le risque de mourir pour les rats-taupes nus ne semble pas augmenter à mesure quils vieillissent; le plus ancien animal non colonial connu au monde, une palourde quahog océanique remarquablement résistante au stress, nommée Ming, nest décédée (accidentellement) quaprès 500 ans lorsque les chercheurs lont draguée hors de locéan et ont voulu savoir quel âge il avait ; les pins bristlecone incroyablement anciens semblent fonctionner aussi bien que les arbres plus jeunes; une colonie particulière de trembles tremblants est considérée comme âgée denviron 80 000 ans… et il existe de nombreuses autres espèces à la longévité inhabituelle qui semblent défier le temps qui passe.
Est-ce quelles détiennent la clé de la jeunesse éternelle pour les humains aussi? Nous savons que le vieillissement chez l’homme est dû à une multitude de facteurs, dont nous ne comprenons pas encore tout à fait. Peut-être que ces exemples dautres espèces peuvent éclairer davantage ces processus.