Empirisk dokumentation tydeliggør risikofaktorer, årsager og første linieinterventioner.
Jeffrey R. Strawn, MD – klinisk instruktør i psykiatri, psykiatrisk afdeling, University of Cincinnati College of Medicine
Paul E. Keck Jr, MD
Professor i psykiatri, afdeling for psykiatri, University of Cincinnati College of Medicine, præsident og administrerende direktør, Lindner Center of HOPE, Cincinnati, OH
Stanley N. Caroff, MD
Professor i psykiatri, afdeling for psykiatri, University of Pennsylvania School of Medicine, chef for indlæggelsespsykiatri, psykiatritjeneste, Philadelphia VA Medical Center
Diagnose og behandling af neuroleptisk malignt syndrom (NMS) er kontroversielt, fordi dette potentielt livstruende syndrom er sjældent, og dets præsentation varierer. Disse faktorer gør det vanskeligt at evaluere behandlinger i kontrollerede kliniske forsøg, og data om den relative effekt af specifikke interventioner er knappe. Det kan dog være muligt at udvikle rationelle behandlingsretningslinjer ved hjælp af empiriske kliniske data.1,2
Denne artikel undersøger bevismateriale relateret til 6 kontroversielle aspekter ved NMS-diagnose og behandling:
• mest pålidelige risikofaktorer
• NMS som en spektrumforstyrrelse
• hvad der forårsager NMS
• NMS udløst af første generation vs anden generation antipsykotika
• første linie interventioner • • genstart af antipsykotika efter en NMS episode.
ER DE PÅLIDELIGE RISIKOFAKTORER FOR NMS? 1) .3-5 Catatonia og organiske hjernesyndromer kan være separate risikofaktorer.1,6
Foreløbige undersøgelser har også impliceret dopaminreceptorabnormiteter forårsaget af genetiske polymorfier eller virkninger af lavt serumjern.1,7, 8 Farmakologiske undersøgelser har antydet, at højere doser, hurtig titrering og IM-injektioner af antipsykotika er forbundet med øget NMS-risiko.3,5 Nogle undersøgelser tyder på, at 15% til 20% af NMS-patienter har haft NMS-episoder.1,2 Derudover har førstegenerations antipsykotika (FGAer) med høj styrke – især haloperidol – antages at have højere risiko end lægemidler med lav styrke og anden generation af antipsykotika (SGAer), selvom denne hypotese stadig er vanskelig at bevise. 9-11
Disse risikofaktorer er imidlertid ikke praktiske til estimering af NMS-risiko hos en given patient, fordi de er relativt almindelige sammenlignet med den lave risiko for NMS-forekomst. For langt størstedelen af patienter med psykotiske symptomer vil fordelene ved korrekt angivet antipsykotisk farmakoterapi opveje risiciene.
Tabel 1 Hvad øger NMS-risikoen?
- Agitation
- Dehydrering
- Udmattelse
- Lav jernkoncentration i serum (normalt: 60 til 170 mcg / dL)
Diagnoser
- Historie af NMS
- Catatonia
- Organiske hjernesyndromer
Centralnervesystem
- Dopaminreceptor dysfunktion
- Basal ganglier dysfunktion
- Sympatisk nervesystem dysfunktion
Farmakologisk behandling *
- Intramuskulære eller intravenøse injektioner
- Dopaminantagonister med høj styrke
- Hurtig dosistitrering
- Høje doser
- FGAer sammenlignet med SGAer (?)
* For individuelle patienter skal disse fælles risikofaktorer afvejes igen fordelene ved antipsykotisk behandling
FGAer: først -generations antipsykotika;
SGAer: anden generations antipsykotika; NMS: neuroleptisk malignt syndrom
Kilde: Referencer 1-5
ER NMS RELATERET TIL PARKINSONISM, CATATONIA ELLER MALIGNANT HYPERTHERMIA?
Parkinsonisme. Nogle forskere har beskrevet NMS som en ekstrem parkinson-krise som følge af overvældende blokering af dopaminveje i hjernen.1,2,12 I denne opfattelse ligner NMS det parkinson-hypertermi syndrom, der kan forekomme hos Parkinsons sygdomspatienter efter pludselig ophør eller tab af effektiviteten af dopaminerg terapi, som kan behandles ved at genindføre dopaminerge stoffer.13 Bevis for at understøtte denne opfattelse inkluderer:
• Parkinsons tegn er et kardinal træk ved NMS.
• Tilbagetrækning af dopaminagonister udfælder syndromet.
• Alle udløsende lægemidler er dopaminreceptorantagonister.
• Risiko for NMS korrelerer med lægemidlers dopaminreceptoraffinitet.
• Dopaminerge agonister kan være en effektiv behandling.
• Læsioner i dopaminerge veje frembringer et lignende syndrom.
• Patienter med NMS har vist lave koncentrationer af cerebrospinalvæske i dopaminmetabolitten homovanillinsyre.14
Catatonia. Fink et al15 og andre16-18 har overbevisende hævdet, at NMS repræsenterer en form for lægemiddelinduceret ondartet katatoni. Bevis der understøtter dette inkluderer:
• De 2 lidelser har neuropsykiatriske symptomer.
• Katatoniske tegn er almindelige i NMS.19
• Malign katatoni og NMS deler fysiologiske tegn og laboratorietegn.20
• Genindførelse af antipsykotika kan forværre begge tilstande akut.
• Benzodiazepiner og elektrokonvulsiv behandling (ECT) ) er effektive behandlinger for begge lidelser. 15-18
Lee21 undersøgte sammenhængen mellem katatoniske træk og behandlingsrespons hos 14 NMS-patienter. De fleste patienter med katatoniske symptomer reagerede på benzodiazepiner, hvorimod ingen af dem havde en ekstrapyramidal-hypertermisk præsentation uden kataton. Lee konkluderede, at NMS er heterogent og kan forekomme i katatoniske og ikke-katatoniske former, der adskiller sig i behandlingsrespons.
Malign hypertermi. Nogle klinikere har sammenlignet NMS med ondartet hypertermi forårsaget af inhalationsanæstetika og succinylcholin.1,2 Bevis inkluderer:
• lignende kliniske tegn på stivhed, hypertermi og hypermetabolisme
• lignende fysiologiske tegn og laboratorietegn, såsom rabdomyolyse
• hypertermi hos begge, der reagerer på dantrolen.
Selv om de 2 er ens i præsentation, opstår malign hypertermi intraoperativt og afspejler en farmakogenetisk lidelse af calciumregulering i skeletmuskulaturen. Derudover reagerer stivhed i malign hypertermi ikke på perifertvirkende muskelafslappende midler.1,22 Beviser tyder på, at patienter, der tidligere har oplevet en NMS-episode, ikke har risiko for ondartet hypertermi.22
HVAD ER PATHOPHYSIOLOGIEN AF NMS?
NMS patofysiologi er kompleks og involverer sandsynligvis samspil mellem flere centrale og systemiske veje og neurotransmittere. Som beskrevet ovenfor tyder overbevisende beviser på, at dopaminblokade spiller en central rolle.12
Dopaminblokade i hypothalamus antages at bidrage til termoreguleringssvigt, og blokade i det nigrostriatale system bidrager sandsynligvis til muskelstivhed og hypermetabolisme. Tabet af dopaminerge input til det forreste cingulate-mediale orbitofrontale kredsløb og det laterale orbitofrontale kredsløb bidrager sandsynligvis til de mentale statusændringer og katatoniske træk set i NMS. 12
Nogle forskere har dog foreslået konkurrerende eller supplerende hypoteser. For eksempel foreslog Gurrera 23, at patienter, der er tilbøjelige til at udvikle NMS, har en sårbarhed over for et hyperaktivt og dysreguleret sympatisk nervesystem, og dette træk – sammen med dopaminsystemforstyrrelse induceret af dopaminblokerende midler – producerer NMS. Andre efterforskere har impliceret serotonin, noradrenalin, gamma-aminosmørsyre og glutaminerge mekanismer. 1,12,24,25
ER FGAS ELLER SGAS LIGERE FOR ÅRSAG NMS?
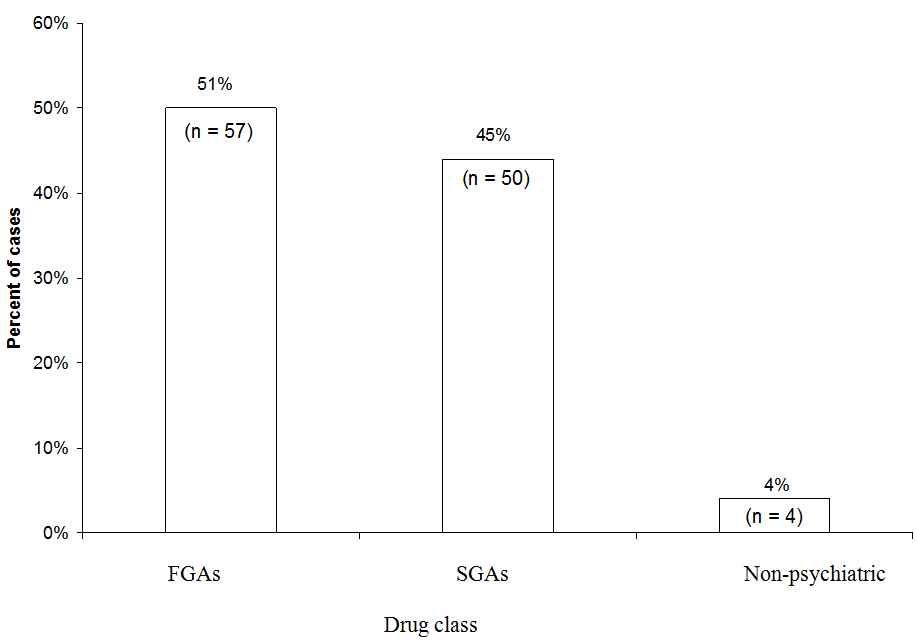
FGA: Første generation antipsykotisk
SGA: Andegenerations antipsykotisk
Lidt flere NMS-tilfælde blev tilskrevet FGAer (51%) end SGAer (45%) i en analyse af 111 tilfælde af sandsynlig eller bestemt NMS forbundet med et enkelt lægemiddel rapporteret til NMS Hotline fra 1997 til 2006. FGA-haloperidol tegnede sig for 44% af alle sager. “Medicinsk” henviser til tilfælde, hvor en neuroleptikum blev brugt i en ikke-psykiatrisk indstilling.
Kilde: Ikke-offentliggjorte data registreret hos Neuroleptic Malignant Syndrome Information Service.
NMS antages at forekomme sjældnere hos patienter behandlet med SGAer end hos dem, der modtager FGAer, skønt denne hypotese er uprøvet. Isolerede rapporter om NMS er blevet forbundet med næsten alle SGA.9-11 Det er vanskeligt at bevise FGA versus SGA-forpligtelser, fordi:
• NMS er sjældent.
• Doseringspraksis kan være mere konservativ nu end tidligere.
• De fleste klinikere er opmærksomme på de tidlige tegn på NMS.
I en epidemiologisk undersøgelse af en stor database fandt Stubner et al 26, at patienter, der fik SGAer, havde en lavere risiko for NMS end dem, der blev behandlet med haloperidol. 26 I denne undersøgelse var den samlede frekvens af NMS 0,02%.
NMS hotline-data. Vi undersøgte for nylig hvilke medicinklasser der var impliceret i 111 NMS-tilfælde rapporteret til Neuroleptic Malignant S yndrome Information Service hotline (1-888-NMSTEMP) mellem 1997 og 2006 (figur). Vi inkluderede kun tilfælde af bestemt eller sandsynlig NMS (som diagnosticeret af hotline-konsulenter), hvor der blev administreret et enkelt antipsykotisk middel. Lidt flere tilfælde blev tilskrevet FGAer (51%) end SGAer (45%). De resterende tilfælde blev tilskrevet neuroleptika, der blev brugt i medicinske omgivelser (såsom promethazin eller prochlorperazin).
Fordi de nu ordineres sjældnere, tegnede FGA sig for et uforholdsmæssigt stort antal NMS-tilfælde rapporteret til hotline. Haloperidol tegnede sig for størstedelen af FGA-sager og 44% af alle sager. Hvis vi havde udelukket haloperidol og sammenlignet NMS-risikoen for SGAer med kun mellemstore eller lavpotente FGAer, ville den relative fordel ved SGAer være gået tabt. På den anden side er det klart, at SGAer stadig bærer en risiko for NMS.
Analyser antyder, at de SGA-associerede klassiske træk ved NMS – feber, muskelstivhed og ændringer i autonom og mental status – bevares hos patienter, der modtager SGAer, selvom nogle måske ikke udvikler den alvorlige stivhed og ekstreme temperaturer, der er almindelige hos patienter, der får FGAer. .9-11 De mildere kliniske egenskaber forbundet med SGAer kan afspejle mere konservative ordineringsmønstre eller øget bevidsthed og tidligere anerkendelse af NMS, hvilket ville forhindre fulminante præsentationer.
HVAD ER BEGIVENHEDEN FOR SPECIFIKKE NMS-BEHANDLINGER?
NMS er sjælden, dens præsentation varierer, og dens progression er uforudsigelig. Disse faktorer gør det vanskeligt at evaluere behandlinger i kontrollerede kliniske forsøg, og data om den relative virkning af specifikke indgreb er knappe.
Alligevel antyder forestillingen om, at NMS repræsenterer en ekstrem variant af lægemiddelinduceret parkinsonisme eller kataton, at specifik NMS behandlinger kan være baseret på symptomens sværhedsgrad eller præsentationsstadiet. Vi foreslår en behandlingsretningslinje baseret på teoretiske mekanismer og anekdotiske data.2,27-29
Support. Efter øjeblikkelig tilbagetrækning af den krænkende medicin er understøttende terapi hjørnestenen i NMS-behandling.1,2,27
For patienter, der har milde tegn og symptomer, kan understøttende pleje og omhyggelig klinisk overvågning være tilstrækkelig. Ekstrem hypertermi kræver volumen genoplivning og afkøling, intensiv lægehjælp og omhyggelig overvågning af komplikationer.
Behandling. På trods af manglende konsensus om lægemiddelbehandling for ukompliceret NMS, modtager ca. 40% af patienterne med akut NMS farmakologiske behandlinger.2
Lorazepam, 1 til 2 mg parenteralt, er en rimelig førstelinjebehandling for NMS, især hos personer med katatoniske træk.4,15-18,21,30,31 Nogle efterforskere anbefaler højere doser.15 Benzodiazepiner foretrækkes, hvis sedation er påkrævet hos agiterede NMS-patienter.4,15-18
Dopaminerge stoffer som bromocriptin og amantadin forbedrer dopaminerge transmission til omvendte parkinsonsymptomer og er rapporteret at reducere tiden til bedring og halvere dødeligheden, når de anvendes alene eller sammen med andre behandlinger.13,27,32,33 Hurtig seponering af disse stoffer kan resultere i reboundsymptomer, skønt dette kan være sandt for enhver specifik lægemiddelbehandling af NMS.1,31,32
Dantrolene afkobler excitation-sammentrækningskobling ved at forbedre calciumbinding i sarkoplasmatisk retikulum i skeletmuskel og har været os ed til at behandle NMS hypermetaboliske symptomer. Nogle anmeldelser fandt forbedring hos op til 80% af NMS-patienter behandlet med dantrolen-monoterapi.27,32-35 Sammenlignet med understøttende pleje kan tiden til bedring reduceres – og dødeligheden faldt med næsten halvdelen – når dantrolen anvendes alene eller i kombination med andre lægemidler.
Ikke alle sagsrapporter har vist, at dantrolen, benzodiazepiner eller dopaminerge agonister er effektive til behandling af NMS.31,36 Efter vores mening er kun avancerede NMS-tilfælde – med ekstreme temperaturforhøjelser, svære stivhed og bevis for systemisk hypermetabolisme – gavn af behandling med dantrolen.1,2
ECT er blevet anvendt med succes til at reducere dødeligheden fra NMS og andre kataton-spektrumforstyrrelser. Det anvendes normalt efter understøttende terapi og psykofarmakologiske indgreb mislykkes.2,15,16,27,37 ECT for akut NMS består typisk af en serie på 6 til 10 behandlinger med bilateral elektrodeplacering. Daglig ECT kan være nødvendig i starten.15
ER ANTIPSYKOTIKA KONTRAINDIKERET FØLGENDE EN NMS-EPISODE?
Hastigheden af NMS-gentagelse ved genbehandling med et antipsykotisk middel har varieret.38 Vi estimerer, at op til 30 % af patienterne kan være i risiko for NMS-tilbagefald, når de genoptages med et antipsykotisk middel.1 Ved at følge passende forholdsregler (tabel 2) kan du dog sikkert behandle de fleste patienter, der har brug for fortsat antipsykotisk behandling.1,2
Når du genstarter behandlingen , kan en antipsykotisk lægemiddel med lavere styrke fra en anden kemisk klasse være en sikrere mulighed end at prøve igen det udløsende middel ifølge retrospektive analyser af begrænsede tilgængelige data. En patient, der udvikler NMS på en FGA, kan drage fordel af et SGA-forsøg, selvom der stadig er en risiko for gentagelse.1,10
Tabel 2 Genindførelse af antipsykotika efter en NMS-episode
Kontroller nøjagtigheden af diagnosen for en tidligere NMS-episode
Dokumentindikationer for antipsykotiske lægemidler
Diskuter risici og fordele, herunder risikoen for gentagelse, med patient og familie
Overvej alternative farmakologiske midler
Minimer risikofaktorer (tabel 1)
Tillad ≥2 uger (≥4 uger for langtidsvirkende injektionsmedicin) efter en NMS-episode er løst inden genudfordring
Vælg FGAer eller SGAer med lav styrke
Ordinere en indledende testdosis
Overvåg vitale tegn og neurologisk status
Titrer doser gradvist
FGAer: første generations antipsykotika;
SGAer: anden generation antipsykotika
Kilde: Referencer 1,2
Relaterede ressourcer
• Informationstjeneste for malignt neuroleptikasyndrom. www.nmsis.org.
• Zarrouf FA, Bhanot V. Malignt neuroleptisk syndrom: Lad ikke din vagt svigte endnu. Nuværende psykiatri 2007; 6 (8): 89-95.
Lægemiddelmærker
Amantadin • Symmetrel
bromocriptin • Parlodel
chlorpromazin • Thorazin og dantrolen • Dantrium®
Fluphenazin • Prolixin
Haloperidol • Haldol
Lorazepam • Ativan
Loxapin • Loxitan
Perphenazin • Trilafon
Prochlorperazin • Compazin, Compro
Promethazin • Phenergan
Thioridazin • Mellaril
Offentliggørelse
Dr. Strawn er et amerikansk psykiatrisk institut for forskning og uddannelse (APIRE) / Janssen Scholar.
Dr. Keck har modtaget forskningsstøtte fra eller fungeret som konsulent til Abbott Laboratories, American Diabetes Association, AstraZeneca Pharmaceuticals, Bristol-Myers Squibb, GlaxoSmithKline, Eli Lilly og Company, Janssen Pharmaceutica, National Institute of Mental Health, National Institute of Drug Abuse, Pfizer , Stanley Medical Research Institute og UCB Pharma.
Dr. Caroff har modtaget forskningsstøtte fra Bristol-Myers Squibb, Ortho-McNeil Neurologics og Pfizer.
- Caroff SN. Neuroleptisk malignt syndrom. I: Mann SC, Caroff SN, Keck PE Jr, Lazarus A, red. Malignt neuroleptisk syndrom og relaterede tilstande 2. udg. Washington, DC: American Psychiatric Publishing Inc; 2003; 1-44.
- Strawn JR, Keck PE Jr, Caroff SN. Neuroleptisk malignt syndrom Am J Psychiatry 2007; 164: 870-6.
- Keck PE Jr, pave HG Jr, Cohen BM, et al. Risikofaktorer for malignt neuroleptisk syndrom Arch Gen Psychiatry 1989; 46: 914-18.
- Rosebush PI, Stewart TD. En prospektiv analyse af 24 episoder af malignt neuroleptisk syndrom Am J Psychiatry 1989; 146: 717-25.
- Berardi D, Amore M, Keck PE Jr, et al. Kliniske og farmakologiske risikofaktorer for malignt neuroleptisk syndrom: en case-control undersøgelse. Biolpsykiatri 1998; 44: 748-54.
- Hvid DA, Robins AH. Catatonia: forbud for det maligne neuroleptiske syndrom Br J Psychiatry 1991; 158: 419-21.
- Rosebush PI, Mazurek MF. Serumjern og malignt neuroleptisk syndrom. Lancet 1991; 338: 149–51.
- Lee JW. Serumjern i kataton og malignt neuroleptisk syndrom Biol Psychiatry 1998; 44: 499-507.
- Ananth J, Parameswaran S, Gunatilake S, et al. Malignt neuroleptisk syndrom og atypiske antipsykotiske lægemidler J Clin Psychiatry 2004; 65: 464-70.
- Caroff SN, Mann SC, Campbell EC. Atypiske antipsykotika og malignt neuroleptisk syndrom Psychiatr Ann 2000; 30: 314-21.
- Hasan S, Buckley P. Nye antipsykotika og det neuroleptiske maligne syndrom Am J Psychiatry 1998; 155: 1113-16.
- Mann SC, Caroff SN, Fricchione G, Campbell EC. Central dopaminhypoaktivitet og patogenesen af malignt neuroleptisk syndrom Psychiatr Ann 2000; 30: 363–74.
- Faktor SA, Santiago A. Parkinsonisme-hyperpyreksi syndrom i Parkinsons sygdom. I: Frucht SJ, Fahn S, red. . Bevægelsesforstyrrelsessituationer: diagnose og behandling. Totowa, NJ: Humana Press; 2005; 29-40.
- Nisijima K, Ishiguro T. Cerebrospinalvæskeniveauer af monoaminmetabolitter og gamma-aminosmørsyre i malignt neuroleptisk syndrom. J Psychiatr Res 1995; 27: 233–44.
- Fink M, Taylor MA. Malignt neuroleptisk syndrom er ondartet kataton, hvilket berettiger til behandlinger, der er effektive for kataton. Prog Neuropsychopharmacol Biol Psychiatry 2006; 30: 1182–3.
- Fricchione G, Bush G, Fozdar M, et al. Anerkendelse og behandling af katatonisk syndrom. J Intensive Care Med 1997; 12: 135–47.
- Philbrick KL, Rummans TA. Ondartet katatoni. J Neuropsychiatry Clin Neurosci 1994; 6: 1–13.
- Mann SC, Caroff SN, Bleier HR, et al. Dødelig kataton. Am J Psychiatry 1986; 143: 1374–81.
- Koch M, Chandragiri S, Rizvi S, et al. Katatoniske tegn i neuroleptisk malignt syndrom. Compr Psychiatry 2000; 41: 73–5.
- Lee JW. Laboratorieresultater. I: Caroff SN, Mann SC, Francis A, Fricchoine GL, red. Catatonia: fra psykopatologi til neurobiologi Washington, DC: American Psychiatric Press, Inc; 2004; 65-75.
- Lee JW.Katatoniske varianter, hyperterme ekstrapyramidale reaktioner og undertyper af malignt neuroleptisk syndrom. Ann Clin Psychiatry 2007; 19: 9–16.
- Caroff SN, Rosenberg H, Mann SC, et al. Malignt neuroleptisk syndrom i perioperativ indstilling. Am J Anesthesiol 2001; 28: 387–93.
- Gurrera RJ. Sympathoadrenal hyperaktivitet og ætiologien af malignt neuroleptisk syndrom. Am J Psychiatry 1999; 156: 169–80.
- Carroll BT. Den universelle felthypotese af kataton og malignt neuroleptisk syndrom. CNS Spectr 2000; 5: 26-33.
- Weller M, Kornhuber J. En begrundelse for NMDA-receptorantagonistterapi af det maligne neuroleptiske syndrom. Med Hypoteser 1992; 38: 329–33.
- Stubner S, Rustenbeck E, Grohmann R, et al. Alvorlige og usædvanlige ufrivillige bevægelsesforstyrrelser på grund af psykotrope lægemidler. Farmakopsykiatri 2004; 37 (suppl 1): S54 – S64.
- Davis JM, Caroff SN, Mann SC. Behandling af malignt neuroleptisk syndrom. Psychiatr Ann 2000; 30: 325–31.
- Adityanjee PA, Singh S, Singh G, Ong S. Spektrum koncept for malignt neuroleptisk syndrom. Br J Psychiatry 1988; 153: 107–11.
- Woodbury MM, Woodbury MA. Neuroleptika-induceret katatoni som et stadium i udviklingen mod malignt neuroleptisk syndrom. J Am Acad Child Adolesc Psychiatry 1992; 31: 1161–4.
- Francis A, Chondragivi S, Rizvi S, et al. Er lorazepam en behandling for neuroleptisk ondartet syndrom? CNS Spectr 2000; 5: 54-7.
- Rosebush PI, Stewart T, Mazurek MF. Behandling af malignt neuroleptisk syndrom. Er dantrolen og bromocriptin nyttige hjælpestoffer til understøttende pleje? Br J Psychiatry 1991; 159: 709-12.
- Sakkas P, Davis JM, Janicak PG, Wang ZY. Narkotikabehandling af det maligne neuroleptiske syndrom. Psychopharmacol Bull 1991; 27: 381–4.
- Rosenberg MR, Green M. Neuroleptisk malignt syndrom: gennemgang af respons på terapi. Arch Intern Med 1989; 149: 1927–31.
- Yamawaki S, Morio M, Kazamutsuri G, et al. Klinisk evaluering og effektiv anvendelse af dantrolennatrium i neuroleptisk malignt syndrom. Kiso to Rinsyou (Clinical Reports) 1993; 27: 1045–66.
- Tsutsumi Y, Yamamoto K, Matsuura S, et al. Behandling af malignt neuroleptisk syndrom ved anvendelse af dantrolennatrium. Psychiatry Clin Neurosci 1998; 52: 433–8.
- Reulbach U, Dutsch C, Biermann T, et al. Håndtering af en effektiv behandling af neuroleptisk malignt syndrom. Crit Care 2007; 11: R4.
- Troller JN, Sachdev PS. Elektrokonvulsiv behandling af malignt neuroleptisk syndrom: en gennemgang og rapportering af sager. Aust N Z J Psychiatry 1999; 33: 650–9.
- Pave HG, Aizley HG, Keck PE Jr, McElroy SL. Malignt neuroleptisk syndrom: langsigtet opfølgning på 20 tilfælde. J Clin Psychiatry 1991; 52: 208-12.