De foto van twee babyapen die zich aan elkaar vastklampen, trok begin vorig jaar kriskras door de wereld. Niet alleen omdat de langstaartapen, Zhong Zhong en Hua Hua, schattig waren, maar ook omdat ze baanbrekend waren: ze waren de eerste primaten die ooit werden gekloond. Geen enkele wetenschapper was er eerder in geslaagd om exacte replicas te maken van dieren zo dicht bij ons in de boom des levens.
Voor sommigen was het beeld iets te dichtbij voor comfort. Lang voordat Dolly het schaap bijna 23 jaar geleden werd gekloond, fantaseerden sciencefictionschrijvers over legers van look-alikes die de rest van de mensheid wegvagen, of klonen die alleen werden gefokt om hun identieke voorouders in stand te houden. Het idee van klonen is verontrustend omdat het in strijd is met het fundamentele morele begrip dat we allemaal verschillend en even waardevol zijn.

Degenen die betrokken zijn bij de wetenschap rond klonen zijn het daarmee eens. Prominente wetenschappers die betrokken zijn bij het klonen, zeggen dat ze nooit de intentie hebben gehad om een persoon te repliceren – en zijn net zo op hun hoede voor het idee als alle anderen. Hun onderzoek dient andere doelen, zeggen ze. Decennialang is het onderzoek naar klonen onderverdeeld in twee gebieden: reproductief klonen, voornamelijk om de veeteelt te verbeteren; en therapeutisch klonen gericht op het kweken van cellen, niet op hele mensen, die kunnen worden gebruikt om ziekten te behandelen.
Tegenwoordig werken slechts een handvol laboratoria wereldwijd aan het klonen, en door andere ontwikkelingen is het nog minder waarschijnlijk dat klonen wordt gebruikt in de toekomst, zeggen onderzoekers. “Mensen houden van deze opwindende, wereldveranderende innovaties, maar er zijn altijd … biologische obstakels die niet zo eenvoudig te overwinnen zijn”, zegt Dietrich Egli, een assistent-professor ontwikkelingscelbiologie aan Columbia University.
Technisch gezien Haalbaar
Bij overdracht van somatische celkern – de technische term voor klonen – wordt een cel gekopieerd door de celkern over te brengen naar een gedoneerde eicel waarvan de eigen celkern is verwijderd. Een snelle elektrische schok stimuleert de eicel om te gaan delen , en omdat de kern uit een volwassen cel komt – en daarom twee strengen DNA heeft in plaats van de enkele streng die normaal in een ei wordt aangetroffen – heeft het geen sperma nodig om een embryo te worden. Na een paar dagen delen, is de massa bestaat uit embryonale stamcellen die theoretisch in staat zijn om een organisme te worden dat genetisch identiek is aan het organisme waar het vandaan komt.
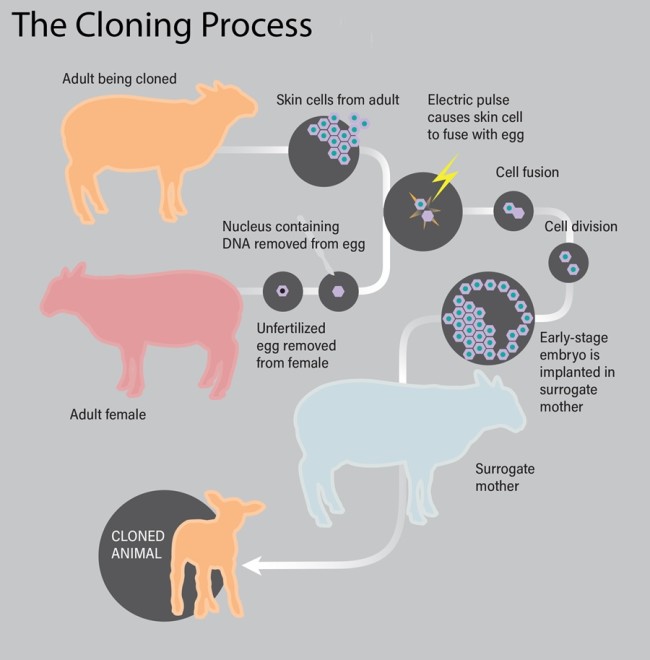
Dus, wat houdt onderzoekers tegen m mensen klonen? Vooral gezond verstand. “Niemand heeft echt een goede reden voorgesteld om het te doen”, zegt Robin Lovell-Badge, een ontwikkelingsbioloog en stamcelwetenschapper aan het Francis Crick Institute in Londen. Er is een veel eenvoudigere manier om jezelf opnieuw te creëren zonder ethische overwegingen. problemen: een baby krijgen. Als je hoopt een geliefd dood kind of overleden echtgenoot na te bootsen, of zelfs een al lang geleden huisdier, zal klonen niet werken. Niet. Werk ”, zegt Lovell-Badge nadrukkelijk. “In feite zou het contraproductief zijn omdat je zou eindigen met een persoon die duidelijk niet dezelfde persoon is, en het zou traumatischer zijn voor alle betrokkenen.”
Beyond Genes
Het punt van Lovell-Badge is dat we allemaal meer zijn dan de genetische handleiding die bij onze creatie betrokken was. We worden gevormd door onze omgeving vanaf de dag van de conceptie: wat onze moeders aten tijdens de zwangerschap en welke virussen ze hebben gevangen, kunnen een impact hebben en niet te vergeten de kwaliteit van het ouderschap of de gebeurtenissen die we tijdens de kindertijd hebben meegemaakt.
Een identieke tweeling onthult dit het beste. Tweelingen hebben vaak verschillende looks, interesses en persoonlijkheden, vooral naarmate ze ouder worden. Plus, sciencefictionfilms (denk aan de film The Island uit 2005) niettegenstaande, zou klonen een baby opleveren, niet een volwassene. Als je genoeg van je overleden echtgenoot houdt om ze na te bootsen, zou je vermoedelijk willen dat hij of zij jouw leeftijd heeft. En, waarschuwt Lovell-Badge, de onvolkomenheden van het klonen kan lijden veroorzaken: Een grote waar Het aantal embryos haalt het niet, pasgeboren klonen sterven soms vlak na de geboorte en andere sterven vroegtijdig. “Het is maar een klein deel dat een gelukkig, lang leven haalt”, zegt Lovell-Badge.
Maar klonen was en kan nog steeds nuttig zijn zonder schattige babys te produceren. leidde tot nieuwe behandelingen voor zeldzame, verwoestende ziekten, zegt Shoukhrat Mitalipov, directeur van de Oregon Health & Science University Center for Embryonic Cell and gentherapie. Hij heeft een manier bedacht om vrouwen met mitochondriale ziekten door de verwoestende ziekte door te geven aan hun kinderen.Door de kern van een van haar eieren over te brengen naar de gezonde eicel van een andere vrouw (wiens kern is verwijderd), kan hij de meeste of alle beschadigde mitochondriën achterlaten, waardoor ziekte wordt voorkomen .Het is een techniek die resulteert in een zogenaamde “drieouderbaby”.
Een vergelijkbare techniek werd in de jaren negentig gebruikt in de VS en sindsdien een paar keer elders om vrouwen met onvruchtbaarheid te behandelen. Nog een “drie -ouderbaby ”werd in 2016 in Mexico geboren met een vergelijkbare techniek die bedoeld was om te voorkomen dat de moeder een ziekte doorgeeft, maar de jongen erfde wel een deel van het beschadigde mitochondriale DNA van zijn moeder, en de familie heeft vervolgonderzoek afgewezen, in de hoop hij zal geen gezondheidsproblemen krijgen.
Een vergelijkbare benadering, door middel van klonen, zou zelfs een vrouw kunnen helpen die zelf geen eieren heeft, zegt Mitalipov. Onderzoekers kunnen mogelijk een van haar huid- of bloedcellen klonen en uiteindelijk een egglittercel maken met een enkele DNA-streng in plaats van een dubbele streng. Vervolgens zou een wetenschapper dezelfde procedure kunnen volgen als bij drieouderbabys om een kind te creëren dat genetisch zowel van haar als van de vader is – dat wil zeggen, een normaal kind, geen kloon. “Dat is waarschijnlijk de toekomst”, zegt Mitalipov.
Concurrenten van klonen
Een ander doel van klonen is altijd geweest om cellulaire therapieën te ontwikkelen, behandelingen die de eigen gekloonde cellen van de patiënt gebruiken. zijn meer geïnteresseerd in gestandaardiseerde therapieën, zegt Egli, en er is nu een veel eenvoudigere manier om gepersonaliseerde multifunctionele cellen te maken zonder eieren of embryos te vernietigen.
Halverwege de jaren 2000 ontwikkelde de Japanse wetenschapper Shinya Yamanaka een methode om kunstmatig te creëren Deze cellen van een volwassene. Yamanaka zegt dat hij door Dolly werd geïnspireerd om te beseffen dat alle cellen hetzelfde genetisch materiaal hebben en dus theoretisch kunnen worden geherprogrammeerd in elk ander celtype. Het besef bracht hem ertoe een methode te ontwikkelen om geïnduceerde pluripotente stamcellen te creëren. (iPSCs) uit volwassen cellen. iPSCs kunnen worden gemaakt om uit te groeien tot elk type weefsel in het lichaam.
Stamcelbioloog Kevin Eggan van de Harvard University zegt dat hij er nu van overtuigd is dat Yamanakas iPSCs vergelijkbaar zijn met gekke e van embryos of van klonen met gedoneerde eieren – zonder de ethische uitdagingen. Deze cellen worden nu over de hele wereld gebruikt in onderzoek voor het modelleren van ziekten en het screenen van medicijnen, en ze beginnen nu pas te worden toegepast bij therapieën, eerst bij maculaire degeneratie. Ze zijn zo gemakkelijk te gebruiken, zegt Eggan, dat zelfs de tweedejaarsstudenten die hij aan Harvard doceert ze kunnen maken.
Maar ondanks het nut van iPSCs en hun overeenkomsten met gekloonde cellen, volgen gekloonde embryos een meer normale ontwikkelingsproces dan die gegenereerd door iPSCs, zegt Lovell-Badge. Mitalipov gelooft dat gekloonde cellen gezondere mitochondriën hebben. En om de een of andere reden kan een gekloonde cel uitgroeien tot een hele muis, terwijl een door iPSC gegenereerd embryo vaak afslaat, zegt Egli van Columbia. Daarom gelooft hij dat klonen nog steeds nodig zijn als referentiepunt voor onderzoek. Toch wordt klonen verdrongen door het gebruik van IPSCs, zegt Lovell-Badge: “Als de iPS-celroute veilig lijkt, betrouwbaar lijkt, waarom zouden mensen dan de technisch veel moeilijkere manier kiezen om het te doen?”
De andere tool die het klonen bijna failliet maakt, is het bewerken van CRISPR-genen. “Als je de embryologie goed genoeg begrijpt om te klonen, begrijp je het goed genoeg om te bewerken”, zegt Eggan. (Zoals alle wetenschappers die in dit stuk worden geciteerd, was Eggan geschokt door het recente gebruik van genbewerking bij tweelingmeisjes in China, een beweging die waarschijnlijk zal leiden tot nieuwe voorschriften voor bewerkingen van menselijke eicellen, sperma en embryos.) populariteit van deze andere technologieën, is er zeer weinig financiering voor onderzoek naar klonen, zegt Egli, en nog minder als het om menselijke cellen gaat.

Niche-technologie
Uiteindelijk kan klonen het nuttigst blijven in het gebied waarvoor het was ontwikkeld: om de veeteelt te verbeteren. Eggan zegt dat wetenschappers 25 jaar geleden niet genoeg wisten over dierlijke genetica om de eigenschappen die ze wilden te versterken en de eigenschappen die ze niet hadden te minimaliseren, dus het klonen van ideale exemplaren leek de beste keuze. Klonen wordt nog steeds voor dat doel gebruikt, vooral voor hoogwaardige dieren, zoals stieren.
Bij sommige dieren, zoals varkens, blijft klonen de meest effectieve manier om gewenste eigenschappen toe te voegen, zegt Angelika Schnieke, voorzitter van biotechnologie voor vee aan de Technische Universiteit van München. Een varkensembryo is gekleurd, waardoor het zelfs met een microscoop bijna onmogelijk is om in het embryo te kijken om genen toe te voegen, zegt ze. Tot nu toe waren er geen iPSC- of embryonale stamcellijnen voor konijnen, varkens of schapen, dus klonen was de enige optie om precieze veranderingen aan te brengen in cellen van die soorten, zegt Schnieke. Klonen kan worden gebruikt om genetische veranderingen die in het laboratorium zijn aangebracht door te geven, waarbij de normale reproductie wordt omzeild. Sommige onderzoekers combineren ook klonen en genoombewerking om bijvoorbeeld varkens te maken die resistent zijn tegen ziekten, zegt ze.
Uiteindelijk zal klonen nooit meer zijn dan een nichetechnologie, zegt Sir Ian Wilmut, de wetenschapper die het klonen van Dolly leidde. Maar hij is meer dan tevreden dat zijn werk heeft geleid tot een nieuw begrip van cellulaire veelzijdigheid en alle voordelen die daaruit voortvloeien. “iPS-cellen zijn verreweg de grootste erfenis van het kloonexperiment”, zegt Wilmut. En hoe zit het met al die angstaanjagende fantasieën om overspoeld te worden door kopieën van onszelf? Of ontdekken dat we alleen in leven zijn om de behoeften van iemand te dienen met onze genetische opmaak? Eggan zegt dat we die nu voor altijd van onze lijst met angsten kunnen schrappen. iPSCs kunnen bijna alles doen wat gekloonde cellen zouden kunnen, zonder de noodzaak voor replicas. “Dat dystopische zicht is nu in de achteruitkijkspiegel”, zegt hij. / p>

Dit verhaal maakt deel uit van “The Future of Fertility”, een nieuwe serie over Discover verkennen van de grenzen van reproductie. Lees meer:
Kunnen mensen babys krijgen in de ruimte?
George Church wil genetische matchmaking tot een realiteit maken
Het bewerken van menselijke genen is controversieel. Shoukhrat Mitalipov is niet afgeschrikt