Is flyter fordi den er mindre tett enn vann. Vann har en tetthet på 1,0 g / kubikk cm.
Tettheten av is Ih er 0,931 g / kubikk cm.
Men hvorfor er is mindre tett enn vann hvis begge er laget opp av molekyler av H2O?
————– > spin on ——– > – spin off
—— > space fill / cpk ——– > pinne —- > ball-and-stick
For å rotere molekylet — > Venstreklikk og dra
For å zoome – > > Venstreklikk + hold nede Skift knappen og dra vertikalt
Jsmol Menu — > > Høyreklikk
Prøv dette!!
Endre til trådramme først:
Klikk på høyre museknapp over ruten
Stil – > Ordninger – – > trådramme
Etikettatomer:
Stil – > Etikett — > atomnummer
Mål følgende vinkler:
< 415
< 512
< 213
< 314
For å måle vinkler: hold venstre musebunn over atom og dobbeltklikk på atom 1, dra til andre atom (midtatom) enkeltklikk sentrum, dra og dobbeltklikk atom 3.
—— > space fill / cpk ——– > stick —- > ball-and-stick
Flytende vann har en delvis ordnet struktur der hydrogenbindinger stadig blir dannet og bryte opp.
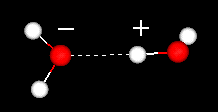
På den annen side har isen en stiv gitterstruktur.
I flytende vann er hvert molekyl hydrogenbundet til omtrent 3,4 andre vannmolekyler.
I is er hvert molekyl hydrogenbundet til 4 andre molekyler.
Sammenlign de to strukturene nedenfor. Legg merke til de tomme plassene i isstrukturen.
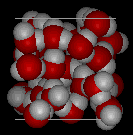 |
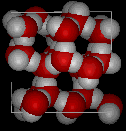 |
I is Ih danner hvert vann fire hydrogenbindinger med O — O avstander på 2,76 Ångstrøm til nærmeste oksygennabo. På grunn av ordnet struktur i is er det mindre H20-molekyler i et gitt volumrom.
Prøv dette –
Prøv dette –
1) Mål OO-avstandene mellom to tilstøtende oksygenatomer i is vist i strukturen ovenfor ..
Vennligst skriv inn svaret ditt i det oppgitte rommet:
I motsetning til is – vann ved romtemperatur er i konstant bevegelse – hydrogenbindinger dannes kontinuerlig og brytes – klikk her for å se vannmolekyler i bevegelse