얼음은 물보다 밀도가 낮기 때문에 뜹니다. 물의 밀도는 1.0 gm / cubic cm입니다.
얼음의 밀도 Ih는 0.931 gm / cubic cm입니다.
그러나 둘 다 만들면 얼음이 물보다 밀도가 낮은 이유는 무엇입니까? 최대 H2O 분자?
————– > 회전 ——– >-스핀 오프
—— > 공백 채우기 / cpk ——– > 스틱 —- > 볼 앤 스틱
분자 회전 — > 왼쪽 클릭 및 드래그
확대 / 축소-> > 왼쪽 클릭 + Shift 키를 누른 상태 버튼을 누르고 수직으로 드래그
Jsmol 메뉴 — > > 오른쪽 클릭
이 시도!!
먼저 와이어 프레임으로 변경 :
상자 위에 마우스 오른쪽 버튼을 클릭
스타일-> 구성표- -> 와이어 프레임
라벨 원자 :
스타일-> 라벨 — > 원자 번호
다음 각도를 측정합니다.
< 415
< 512
< 213
< 314
각도를 측정하려면 : 원자 위에 마우스 왼쪽 버튼을 누른 상태에서 원자 1을 두 번 클릭하고 두 번째 원자 (가운데 원자)로 드래그 한 다음 중심 원자를 한 번 클릭 한 다음 원자 3을 드래그하고 두 번 클릭합니다.
—— > 공백 채우기 / cpk ——– > 스틱 —- > 볼앤 스틱
액체는 수소 결합이 지속적으로 형성되고
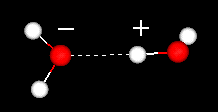
반면 얼음은 단단한 격자 구조를 가지고 있습니다.
액체 물에서 각 분자는 약 3.4 개의 다른 물 분자에 수소 결합됩니다.
얼음에서 각 분자는 4 개의 다른 분자에 수소 결합됩니다.
아래의 두 구조를 비교하세요. 얼음 구조물 내의 빈 공간을 확인하십시오.
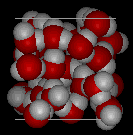 |
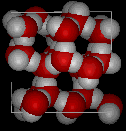 |
얼음 Ih에서는 각 물이 형성됩니다. 가장 가까운 산소 이웃에 2.76 옹스트롬의 O — O 거리를 가진 4 개의 수소 결합. 얼음의 질서있는 구조로 인해 주어진 부피 공간에 H20 분자가 더 적습니다.
사용해보세요-
사용해보세요-
1) 측정 위 구조에 표시된 얼음에서 인접한 두 산소 원자 사이의 OO 거리 ..
제공된 공간에 답을 입력하세요.
얼음과 달리-상온의 물은 일정하게 움직입니다-수소 결합은 지속적으로 형성되고 끊어집니다. 물 분자가 움직이는 것을 보려면 여기를 클릭하십시오.