Jarisch-Herxheimer 반응 (JHR) 또는 “herxing”은 1800 년대 후반에 의사들에 의해 처음 설명되었습니다.이 현상을 경험 한 환자는 발병 직후 비특이적 증상이 증가했다고보고합니다. 이러한 증상은 오한, 발열, 두통 및 / 또는 피부 발진의 심화를 포함합니다. 1 세기 이상 전에 설명 되었음에도 불구하고 연구자와 의사가 JHR 및 그 변이로 이어지는 병원성 메커니즘을 설명하는 것은 여전히 어렵습니다. 환자 감수성에서.
오스트리아와 독일의 피부과 의사 인 Adolf Jarisch 박사와 Karl Herxheimer 박사가 매독 환자에서 JHR을 처음으로 설명했습니다. 그들은 매독 관련 피부 병변이 곧 악화된다는 점을 지적했습니다. 수은 화합물로 치료를 시작한 후 며칠 후 병변이 해결되기 시작했습니다. 그 당시에는 수은이나 다른 것의 존재가 초기의 원인 일 수 있는지 확실하지 않았습니다. l 부정적인 반응
안전하고 효과적인 항생제 인 페니실린이 1940 년대에 시장에 출시되었을 때 매독 감염에 대한 치료법이되었습니다. 그러나 일부 환자는 치료 시작 후 24 시간 이내에 증상이 악화되었다고보고했습니다. 또한 테트라 사이클린, 클라리 트로마 이신 및 아지트로 마이신을 포함하여 현재 일반적으로 사용되는 다양한 최신 항생제가 라임 병, 렙토스피라증 및 진드기 매개 재 발열 (TBRF)의 경우 JHR을 유발하는 것으로 나타났습니다. 2015 년 사례 보고서에는 안면 홍조 및 불쾌감을 포함한 JHR 증상을 경험 한 후 독시사이클린 치료를 중단해야했던 라임 병에 대해 CDC 양성인 여성이 설명되어 있습니다.
JHR의 원인은 무엇입니까?
매독, 라임 병, 렙토스피라증 및 TBRF를 연결하는 공통된 원인은 모두 스피 로체 테 가족에 속하는 박테리아에 의해 발생한다는 사실입니다. 스피 로체 테과는 상대적으로 작지만 코르크 모양의이 박테리아는 인간의 삶에 엄청난 영향을 미칩니다. 라임 병의 원인균 인 Borrelia burgdorferi는 유행이 증가하고 있기 때문에 현재 아마도 가장 잘 알려진 스피 로체 테일 것입니다. 매독은 Treponema pallidum에 의해 발생하며 사람들간에 성적으로 전염됩니다.
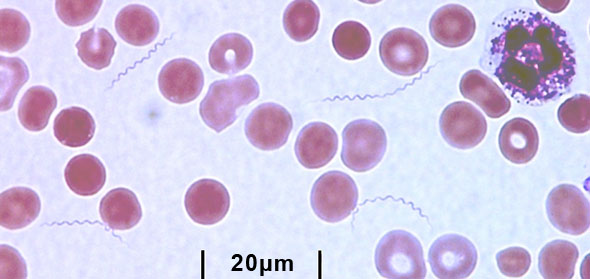
연구에 따르면 항생제 치료가 유발 될 수있는 두 가지 주요 이유가 있습니다. 일부 환자의 JHR.
세포 구성 요소
임상 인들은 일단 죽으면 체내로 방출되는 스피로 체트에 내 독소가있을 수 있다고 처음으로 의심했습니다. Bacillus anthracis (anthrax)와 같은 많은 박테리아는 방어 메커니즘으로 이러한 유형의 독소를 생성합니다. 그러나이 스피로 체트는 인간에게 생물학적으로 활성이있는 독소가없는 것으로 밝혀졌습니다. 대신 연구원들은 남아있는 세포의 고유 한 구성 요소가 염증 반응을 유발할 수 있음을 발견했습니다.
T. pallidum에서 지단백질 (세포 표면 단백질)은 인간 대 식세포에서 종양 괴사 인자 (TNF) 생성을 자극하는 것으로 밝혀졌습니다. . TNF의 생성은 근육과 다른 조직을 손상시키는 불필요한 염증 반응을 일으킬 수 있습니다. 웨스턴 블롯 테스트의 표적 중 하나 인 Borrelia burgdorferi의 외부 표면 단백질 A (OspA)는 세포 배양에서 사이토 카인 반응을 증가시키는 것으로 나타났습니다. 2019 년에 연구자들은 주요 세포벽 구성 요소 인 펩티도 글리 칸을 라임 관절염의 지속 가능한 원인으로 확인했습니다.
면역 반응 상승
다음을 포함한 숙주 면역 반응 및 염증 매개체 사이토 카인, 히스타민 및 백혈구는 모두 JHR과 관련이 있습니다. 연구에 따르면 항생제 치료는 일부 환자에게 문제를 일으킬 수있는 단기 면역 반응을 일으킬 수 있습니다.
Borrelia burgdorferi 및 기타 Borrelia 종에 대한 연구에 따르면 백혈구는 다음과 같은 염증 반응을 증가시킬 수 있습니다. 박테리아의 섭취. 백혈구의 수용체는 다른 곳에서 부적절한 염증을 유발하는 사이토 카인 반응을 유발할 수 있습니다. IL-6 및 IL-8과 같은 사이토 카인은 재발 성 열에 대한 페니실린 치료 후 2 시간 이내에 증가하는 것으로 나타났습니다. 또한 JHR은 Borrelia 세포 제품을 섭취 한 후 백혈구의 세포 사멸 (프로그래밍 된 세포 사멸)로 인해 발생할 수 있습니다.
JHR 대 기타 치료 증상
JHR 유사 반응은 spirochetes가 아닌 감염의 치료에보고되었습니다. 특히, 일부 Bartonella 종 감염 환자는 항생제 치료를 시작할 때 증상이 악화되는 것을 느낀다고보고합니다. 무슨 일이야?이러한 치료 증상은 잘 연구되지 않았지만 항생제가 신체에 다양한 영향을 미친다는 증거가 있습니다. 원인 중 일부는 표적 박테리아와 숙주 면역 세포 모두에서 세포 폐기물의 증가와 같이 유사 할 수 있습니다. 그들은 숙주 자체에 영향을 주어 숙주 세포의 기능을 변화시킬 수 있습니다. 그들은 또한 미생물 군유 전체를 변화시켜 숙주 세포가받는 대사 산물을 갑작스럽게 변화시킵니다. 물론 그 미생물 군집의 일부 세포는 그 자체로 스피 로체 테입니다.
2017 년에 Bacillary angiomatosis와 HIV가있는 Bartonella quintana를 앓고있는 한 남성의 사례 연구에서 치료 중 면역 재구성 염증 증후군을 경험했다고보고했습니다. (IRIS) 및 JHR. 이러한 반응은 그가 HIV에 대한 항 레트로 바이러스 요법과 바르 토넬 라증에 대한 항생제를 투여 받으면서 발전했습니다. 저자는 환자가 치료를 시작한지 하루 이내에 발진의 형태로 JHR을 경험했으며 항생제 중단 후 약 이틀 후에 더 심한 증상을 경험했다고 말합니다. spirochetes는 일반적으로 JHR과 관련이 있지만, 다른 박테리아 군은 환자의 미생물 부담이 높을 때 유사한 반응을 일으킨다는 증거가 있습니다. 이 사례 보고서는 인터넷에서 무료로 읽을 수 있습니다.
결론
항생제 치료를받은 환자가 기분이 나아지기 전에 기분이 나 빠졌다고보고하는 것은 드문 일이 아닙니다. 이러한 증상은 매독 환자에서 가장 면밀히 연구되어 감염원이 스피로 체트 일 때 원인에 대한 다양한 이론으로 이어집니다. 그러나 100 년 이상의 관찰에도 불구하고 spirochetes의 경우에도 치료 증상의 정확한 원인이 확인되지 않았습니다.