화학 원소 인 란탄은 란탄 족과 희토류 금속으로 분류됩니다. 1839 년 Carl G. Mosander가 발견했습니다.

데이터 영역
| 분류 : | 란탄은 란탄 족 및 희토류 금속입니다. |
| 색상 : | 은백색 |
| 원자 무게 : | 138.9055 |
| 상태 : | 고체 |
| 녹는 점 : | 1540oC, 1813.2K |
| 끓는점 : | 2830oC, 3103K |
| 전자 : | 57 |
| 양성자 : | 57 |
| 가장 풍부한 동위 원소의 중성자 : | 82 |
| 전자 껍질 : | 2,8,18,18, 9,2 |
| 전자 구성 : | 5d1 6s2 |
| 밀도 @ 20oC : | 6.16 g / cm3 |
열, 에너지, 산화,
반응을 포함하여 자세히 표시 , 화합물, 반경, 전도도
| 원자 부피 : | 22.5 cm3 / mol |
| 구조 : | hcp : 육각형 마감 패킹 |
| 경도 : | 2.5 mohs |
| 비열 | 0.19 J g-1 K-1 |
| 융해열 | 6.20 kJ mol-1 |
| 무화 열 | 414 kJ mol-1 |
| 증발 | 400kJ mol-1 |
| 1 차 이온화 에너지 | 538.1 kJ mol-1 |
| 2 차 이온화 에너지 | 1067 kJ mol-1 |
| 3 차 이온화 에너지 | 1850 kJ mol-1 |
| 전자 친 화성 | 50kJ mol-1 |
| 최소 산화수 | 0 |
| 최소 일반적인 산화 번호 | 0 |
| 최대 산화 수 | 3 |
| 최대. 일반적인 산화 번호. | 3 |
| 전기 음성도 (폴링 스케일) | 1.1 |
| 분 극성 부피 | 31.1 Å3 |
| 공기와의 반응 | 격렬함, w / ht ⇒ La2O3 |
| 15M HNO3와의 반응 | 온화함, ⇒ La (NO3) 3 |
| 6M HCl과의 반응 | 마일드, ⇒ H2, LaCl3 |
| 6M NaOH와의 반응 | 없음 |
| 산화물 ( s) | La2O3 |
| 수 소화물 | LaH2, LaH3 |
| 염화물 | LaCl3 |
| 원자 반경 | 195 pm |
| 이온 반경 (1+ 이온) | – |
| 이온 반경 (2+ 이온) | – |
| 이온 반경 (3+ 이온) | 117.2 pm |
| 이온 반경 (1- 이온) | – |
| 이온 반경 (2- 이온) | – |
| 이온 반경 (3- 이온) | – |
| 열 전도도 | 13.4 W m-1 K-1 |
| 전기 전도도 | 1.9 x 106 S m-1 |
| 어는점 / 어는점 : | 1540 oC, 1813.2 K |

Lanthanum은 스튜디오 조명, 노트북 배터리, 카메라 렌즈 및 하이브리드 자동차 배터리.
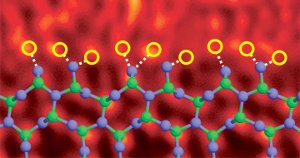
질화규소 입자 경계 도핑 란탄 원자로. 이미지 참조. (6)
란탄의 발견
Lanthanum은 1839 년 Carl G. Mosander가 스웨덴 스톡홀름의 광물 cerite에서 발견했습니다.
Ceria (산화 세륨)는 스웨덴 화학자 Jacob에 의해 1803 년에 이미 발견되었습니다. 미네랄 cerite의 Berzelius. Berzelius의 학생 중 한 명이었던 Mosander는 세리아가 다른 희토류를 포함하는 불순한 산화물이라고 의심했습니다. (1)
모산 더는 미세하게 분말 화 된 질산 세륨을 취하고 차갑게 희석 된 질산을 첨가했습니다. 산에 용해 된 질산 세륨 분말 중 일부는 새로운 지구가 존재할 수 있음을 나타냅니다. 새로운 산화물은 세리아 (세륨 산화물)보다 더 염기성이며 세리아와 달리 산에 용해되었습니다. Mosander는 수산 나트륨과 열을 사용하여 침전물에서 용액을 분리했습니다. 그는 새로운 희토류의 옅은 벽돌색 산화물을 얻었다. (1)
새로운 산화물의 이름 lanthana는 그의 친구 Berzelius가 제안했습니다.
이 이름은 숨겨진 의미의 그리스어 lanthano에서 유래했습니다.
Axel Erdmann은 새로 발견 된 노르웨이 광물에서 Mosander와 같은 해에 독립적으로 란타늄을 발견했습니다. Erdmann은 Mosander를 기리기 위해 새로운 광물 mosandrite라고 불렀습니다.(2)
Mosander는 염화물로부터 불순한 금속성 란탄을 얻었다. (1)
순수 란탄 금속은 1923 년 H. Kremers와 R. Stevens가 융합 할로겐화물을 전기 분해하여 처음으로 생산되었습니다.
Mosander는 란타나를 계속 연구했으며 1841 년에 발견을 발표했습니다. 그 안에 포함 된 또 다른 희토류의. 그는 란탄의 뗄래야 뗄 수없는 쌍둥이 형제 인 것처럼 보였기 때문에 디디 뮴이라고 명명했습니다. (2)
디디 뮴은 나중에 별도의 발견에서 알려지지 않은 희토류 원소의 혼합물로 밝혀졌습니다. 1879 년 Lecoq de Boisbaudran은 디디 뮴에서 사마륨을 발견하고 그로부터 사마륨을 분리했습니다. Carl Auer von Welsbach는 1885 년에 남아있는 디디 뮴이 실제로 네오디뮴과 프라세오디뮴이라는 두 가지 완전히 새로운 요소의 혼합물임을 발견했습니다.


Lanthanum은 일부 풀 제품에 사용되어 공급되는 인산염 영양소 수준을 줄입니다. 조류.

상단 중앙에서 시계 방향으로 : 프라세오디뮴, 세륨, 란타늄, 네오디뮴, 사마륨 및 가돌리늄의 희토류 산화물. 사진 : LLNL
외관 및 특성
유해 영향 :
란탄과 그 화합물 약간의 독성이있는 것으로 간주됩니다.
특성 :
란탄은 은백색의 연질 금속으로 칼로자를 수 있습니다.
연성이 있습니다. , 가단성 및 노출 된 표면은 공기 중에 빠르게 변색되어 산화물을 형성합니다.
란탄은 물과 반응하여 수산화 란탄과 수소 가스를 형성합니다.
란탄은 화학적으로 반응하며 탄소, 질소와 화합물을 형성합니다. , 붕소, 셀레늄, 실리콘, 인, 황 및 할로겐.
란탄은 일반적으로 화합물에 3가 이온 La3 +로 존재합니다.
란탄의 용도
란탄은 하이브리드 자동차 용 니켈 금속 수 소화물 (NiMH) 2 차 전지에 대량으로 사용됩니다. NiMH 배터리의 음극 (음극)은 금속 수 소화물의 혼합물입니다.이 중 하나는 일반적으로 란탄 수 소화물입니다. 음극의 활성 물질은 수소이며 금속 수 소화물 구조에 저장됩니다. 금속 수 소화물은 조성에 따라 수소를 1 ~ 7 중량 % 보유 할 수 있습니다. (3) Toyota Prius 배터리에는 약 10kg의 란탄이 필요합니다. (4)
란탄은 석유 분해 촉매로 사용되며 장쇄 탄화수소를 짧은 사슬 종으로 분할하는 촉매제입니다.
란탄은 구상 주철을 만드는 첨가제로 사용됩니다. 강철의 첨가제로.
화염 라이터 부싯돌은 란탄이 포함 된 미시 금속 (희토류 합금)을 사용하여 마찰에 의해 스파크를 생성합니다.
란탄은 자체적으로 최대 400 배를 차지하는 수소 스폰지 합금에 사용됩니다. 란탄은 야간 투시경 (적외선 흡수 유리)을 만드는데도 사용됩니다.
고품질 카메라 및 망원경 렌즈에는 산화 란탄 (La2O3)이 포함되어 있습니다. 굴절률이 높고 분산이 적습니다.
란탄 탄산염은 신장 질환 환자의 혈중 인산염 수치를 낮추는 데 사용됩니다. (5)
란탄 화합물은 조류가 먹는 인산염 영양소 수준을 낮추기 위해 일부 풀 제품에도 사용됩니다.
풍부 및 동위 원소
풍부한 지각 : 중량 기준으로 34ppm, 몰 기준으로 5ppm
풍부한 태양계 : 10 억분의 2 무게, 0.01 몰당 0.01 부
순도 비용 : 100g 당 $ 800
비용, 부피 : 100g 당 $
출처 : 란탄은 공짜로 발견되지 않습니다. 자연에서. 주로 미네랄 모나자이트와 바스 네 사이트에서 발견됩니다. 상업적으로 다양한 복합 추출 기술을 사용하여 모나자이트 모래와 바스 나에 사이트에서 회수됩니다. 순수한 란탄은 칼슘 금속으로 불소를 환원시켜 얻습니다.
동위 원소 : 란탄에는 반감기가 알려진 31 개의 동위 원소가 있으며 질량 수는 119 ~ 150입니다.이 중 하나는 139La입니다. 자연적으로 발생하는 란탄은 각각 0.09 %와 99.91 %의 자연 풍부도를 가진 두 동위 원소 138La와 139La의 혼합물입니다.

이 페이지 인용
온라인 링크의 경우 다음 중 하나를 복사하여 붙여 넣으십시오.
<a href="https://www.chemicool.com/elements/lanthanum.html">Lanthanum</a>
또는
<a href="https://www.chemicool.com/elements/lanthanum.html">Lanthanum Element Facts</a>
학술 문서에서이 페이지를 인용하려면 다음 MLA 준수 인용을 사용하세요.
"Lanthanum." Chemicool Periodic Table. Chemicool.com. 17 Oct. 2012. Web. <https://www.chemicool.com/elements/lanthanum.html>.