Der Begriff aberrante Leitung bezieht sich auf eine vorübergehende Verzweigungsblockade, die nicht auf frühere QRS-Anomalien, die Leitung des Nebenwegs oder unerwünschte Arzneimittelwirkungen zurückzuführen ist. 1 Die Blockade kann auf jeder Ebene des His-Purkinje-Systems auftreten und auf unterschiedliche Mechanismen zurückzuführen sein. Der Block der Phase 3 (Tachykardie-abhängig) ist auf das Eindringen von Gewebe während der effektiven Refraktärzeit zurückzuführen und kann ein physiologisches oder pathologisches Phänomen sein. Eine spezielle Form dieses Blocks ist der beschleunigungsabhängige Block, der auf Änderungen der Herzfrequenz zurückzuführen ist. Der Block der Phase 4 (Bradykardie-abhängig oder pausenabhängig) ist fast immer pathologisch. Es tritt nach dem Ende der Refraktärperiode aufgrund eines verringerten Membranpotentials aufgrund einer erhöhten His-Purkinje-Automatik oder einer teilweisen Depolarisation der Myokardläsion auf. Der vierte und letzte aberrante Mechanismus beruht auf einer verborgenen Leitung, die als Ausbreitung eines Impulses innerhalb des spezifischen Leitungssystems definiert ist und nur an seiner Auswirkung auf den Impuls, das Intervall oder die folgenden Zyklen erkannt werden kann.2 Wie durch angezeigt Dieses Phänomen kann im Oberflächen-Elektrokardiogramm (EKG) nicht beobachtet werden.
Wir stellen den Fall einer 86-jährigen Frau vor, die wegen Herzklopfen und Atemnot in die Notaufnahme eingeliefert wurde. Einige Jahre zuvor war sie von einem Kardiologen auf asymptomatische Sinusbradykardie untersucht worden, für die sie keine Behandlung erhielt. Die körperliche Untersuchung ergab unregelmäßige Herzgeräusche geringer Intensität ohne Murmeln und bibasales Knistern ohne weitere interessante Befunde. Bei der Aufnahme zeigte das EKG Vorhofflimmern mit einer ventrikulären Reaktion von etwa 100 Schlägen pro Minute, wobei sich der linke vordere Faszikularblock (LAFB) mit Schlägen mit einem engeren QRS-Komplex abwechselte (Abbildung 1A und Abbildung im Zusatzmaterial). Während ihres Aufenthalts in der Notaufnahme wurden der Patientin 2,5 mg Atenolol intravenös verabreicht und sie erreichte einen Sinusrhythmus mit einer Geschwindigkeit von 39 Schlägen pro Minute bei Normalisierung der QRS-Morphologie (Abbildung 1B und Abbildung im Zusatzmaterial). Der Patient wurde ohne antiarrhythmische Medikamente entlassen. Mit 3 Wochen wurde sie mit ausgeprägter Asthenie aufgenommen und dokumentierte eine Sinusbradykardie bei 35 Schlägen pro Minute, für die sie einen DDD-Schrittmacher erhielt.
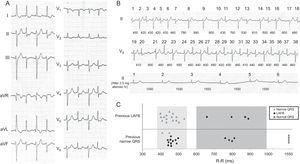
A: Elektrokardiograph mit 12 Ableitungen. B: Vollständige EKG-Verfolgung bei Aufnahme. Die Beats 1–38 sind aufeinanderfolgend, obwohl sie sich in zwei verschiedenen Leads befinden (II und V5). Die Zykluslängen zwischen den Schlägen werden in Millisekunden angezeigt. Das untere Feld zeigt die QRS-Morphologie nach intravenöser Verabreichung von 2,5 mg Atenolol und Umwandlung in den Sinusrhythmus. C: Die Beziehung der QRS-Morphologie zur Zykluslänge und zur Morphologie des vorhergehenden Schlags. LAFB, linker vorderer Faszikelblock.
Eine sorgfältige Analyse des EKG während der Episode ergab eindeutig zwei Arten von QRS: a) QRS mit LAFB-Morphologie (120 ms), abwechselnd mit b) schmalem QRS mit kleinem Variationen in Achse und Dauer (90–100 ms). Darüber hinaus hatten Beats in längeren R-R-Intervallen immer eine LAFB-Morphologie. In Abbildung 1C können zwei Bereiche klar unterschieden werden, in denen die Morphologie des QRS mit der Zykluslänge und dem vorherigen QRS-Komplex verglichen wird.3 In Zone 1 (R – R, 400–530 ms) hängt die QRS-Morphologie vom vorherigen Schlag ab (dh wenn der vorherige Schlag eng ist, hat der folgende Schlag eine LAFB-Morphologie). Die einzigen Ausnahmen von dieser Regel sind die Schläge 32–33, die durch das Eindringen des Impulses in die übernormale Leitungsphase des vorderen Faszikels erklärt werden könnten.3,4 In Zone 2 (R – R > 600 ms) hat der QRS-Komplex immer eine LAFB-Morphologie, unabhängig von der Morphologie des vorherigen Schlags, was auf einen Bradykardie-abhängigen Block hindeutet. Der merkwürdige Aspekt dieses Falles ist, dass im Gegensatz zu dem, was bei diesem Blocktyp zu erwarten wäre, nach einem viel längeren RR-Intervall (> 1500 ms) das QRS normal wird / p>
Abbildung 2 zeigt den vorgeschlagenen Mechanismus für diese Ergebnisse. Bei kurzen R-R-Intervallen (Zone 1) tritt im anterioren Faszikel ein anterograder und retrograder Block auf, der den folgenden Impuls anterograd leiten lässt, da er Zeit zur Repolarisation hat. Auf diese Weise könnten die kleinen Variationen in engen QRS-Komplexen durch ihr Auftreten zu unterschiedlichen Zeitpunkten in ihrer relativen Refraktärperiode mit einem höheren oder niedrigeren Latenzgrad (z. B. Schläge 3 und 7 oder 13 und 15) erklärt werden. Bei sehr langen Zykluslängen finden eine Gewebewiederherstellung und eine permanente anterograde Überleitung statt. Cohen et al. 5 beschrieben dieses Phänomen Ende der 1970er Jahre und nannten es Pseudobradykardie-abhängige Verzweigungsblock-Alternans (dh einen Phase-3-Block).Damit dies geschieht, sollte die retrograde effektive Refraktärperiode des vorderen Faszikels kürzer sein als die anterograde effektive Refraktärperiode und daher eine versteckte retrograde Überleitung begünstigen.4
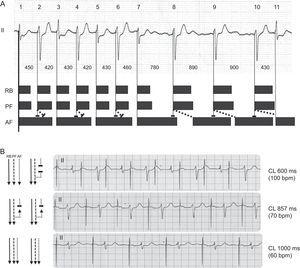
A. Vorgeschlagener Mechanismus der elektrokardiographischen Befunde. Schwarze Balken repräsentieren die theoretisch effektiven Refraktärperioden, und schräge gepunktete Linien repräsentieren versteckte retrograde Grenzflächenleitung. B. Bestätigung des Mechanismus mit atrialer Stimulation (AAI). AF, vorderer Faszikel; CL, Zykluslänge; PF, hinterer Faszikel; RB, rechter Zweig.
Wir konnten diesen Mechanismus bestätigen (Abbildung 2B), da unserem Patienten ein DDD-Schrittmacher implantiert worden war. Alternierendes LAFB wurde durch AAI-Stimulation bei 100 Schlägen pro Minute erzeugt, bei 70 Schlägen pro Minute wurden alle Schläge mit LAFB-Morphologie durchgeführt, und bei 60 Schlägen pro Minute waren alle Schläge eng, was eine Tachykardie-abhängige Blockade bestätigte