Unter den Arten von allergischen Augenerkrankungen wurde neben saisonalen Allergien und frühlingshafter und atopischer Keratokonjunktivitis traditionell auch die Riesen-Papillen-Konjunktivitis (GPC) eingeschlossen. Wir wissen jetzt jedoch, dass GPC eine solche Klassifizierung nicht verdient. Was wir historisch als allergische Reaktion angesehen haben, ist das Ergebnis einer chronischen Reizung, die mit Kontaktlinsenkanten, Prothesen oder Nähten verbunden ist. Obwohl unser Wissen über GPC seit seiner ersten Identifizierung fortgeschritten ist, bleibt die alte Kategorisierung bestehen.
Neben dieser falschen Klassifizierung bleibt GPC auch bei der falschen Nomenklatur hängen. GPC ist weder wirklich riesig noch papillär. In einigen Fällen wird die Erkrankung als kontaktlinseninduzierte papilläre Konjunktivitis bezeichnet, aber viele Augenärzte nennen sie immer noch GPC. Und obwohl es sich um eine Bindehautentzündung handelt, könnte sie besser als Tarsitis bezeichnet werden. Eine genaue Beschreibung wäre Miniatur holpriger oberer Tarsus.
Besprechen Sie hier, wie Sie diesen häufig falsch gekennzeichneten und missverstandenen Zustand richtig diagnostizieren und behandeln können.
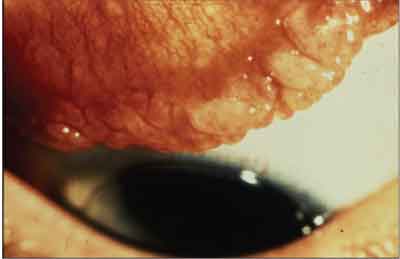
Eine riesige papilläre Konjunktivitis ist keine allergische Reaktion. Obwohl es sich um eine Bindehautentzündung handelt, wäre eine genauere Beschreibung der holprige obere Fußwurzelknochen.
Die Wurzel des Problems
GPC tritt auf, wenn die Hyperaktivität von Mastzellen und anderen Immunzellen hyperaktiv ist Förderung des Kollagenwachstums zur Bildung von Bindehautpapillen.1 Dieses Wachstum unterscheidet die Papillen in GPC von denen, die bei bakterieller Konjunktivitis beobachtet werden. Obwohl dieser pathophysiologische Mechanismus auch bei der frühlingshaften Keratokonjunktivitis (VKC) zu finden ist, die eine echte allergische Erkrankung darstellt, ist GPC keine allergische Reaktion. Bei einer Augenallergie sind die Spiegel von Histamin, Eosinophilen und eosinophilem Hauptgrundprotein erhöht; Dies ist bei GPC.1 nicht der Fall.1
GPC ist vielmehr eine proliferative Reaktion auf ein chronisches, physisches Trauma. Die Dauer und Art des Stimulus, der diese mechanische Reizung hervorruft, kann auch die Präsentation und den Schweregrad der GPC bestimmen.
GPC entsteht am häufigsten durch Kontaktlinsenverschleiß. Die Wurzel des Problems ist die Linsenkante, die am Auge reibt, wenn sie 8.000 Mal pro Tag blinkt. Dies führt zu chronischen Reizungen, die zu Entzündungen führen. Das Überwiegen von GPC bei Kontaktlinsenträgern wurde ursprünglich auf eine Allergie gegen Linsenpolymer oder Ablagerungen zurückgeführt, was zu einer Fehlkategorisierung der Bedingungen als Allergie beitrug.2
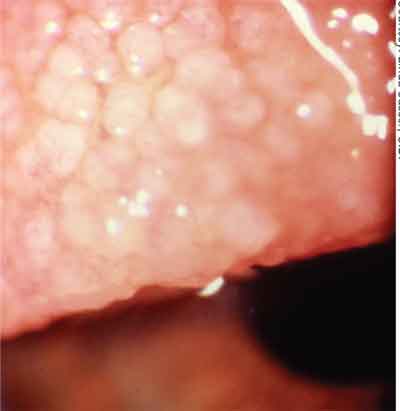
GPC resultiert aus chronischen mechanischen Reizungen an einer Kontaktlinsenkante, einer Skleraschnalle oder einer Naht, die eine Entzündung der Fußwurzelbindehaut verursachen.
Anzeichen und Symptome
Die charakteristischen Riesenpapillen von GPC machen den Zustand leicht identifizierbar. Obwohl der Name der Krankheit etwas anderes impliziert, haben Papillen von GPC typischerweise einen Durchmesser von nicht mehr als 0,3 mm; Dies ist kleiner als die > 1-mm-Papillen, die in VKC zu sehen sind. Papillen in GPC, die durch weiche Linsen induziert werden, beginnen typischerweise in der oberen Zone der Fußwurzelbindehaut und schreiten zum Lidrand hin fort; Sie haben schließlich ein gleichmäßig verteiltes Muster über die Fußwurzelbindehaut.
Papillen sind bei gasdurchlässigen Linsenträgern nicht so zahlreich. Wenn sie auftreten, haben sie eine kraterartigere Form. Die Position der Papillen unterscheidet sich ebenfalls; Diejenigen, die durch GP-Linsen induziert werden, bilden sich zuerst in der Nähe des Lidrandes der Fußwurzelbindehaut.
Der Beginn der GPC kann zwischen einigen Wochen und einigen Jahren nach Beginn des Kontaktlinsenverschleißes auftreten und ist typischerweise bilateral, da die Ursache (Kontaktlinsenverschleiß) typischerweise bilateral ist. GPC kann einseitig sein, wenn die Quelle der Reizung nicht Kontaktlinsen sind, sondern eine Abnormalität wie eine Naht, die ebenfalls einseitig ist.
Zusätzliche Anzeichen und Symptome von GPC sind Risse, Fremdkörpergefühl, leichte bis mittelschwere Hyperämie und fadenförmige oder blattartige Schleimproduktion. Juckreiz, ein Kennzeichen für echte allergische Zustände, fehlt bei GPC im Allgemeinen, und die für VKC typischen Schildgeschwüre oder andere Hornhautbeteiligungen treten bei GPC nicht auf. Das Ziehen am oberen Deckel führt bei GPC-Patienten aufgrund der entzündlichen Infiltration in diesem Bereich zu erheblichen Beschwerden.
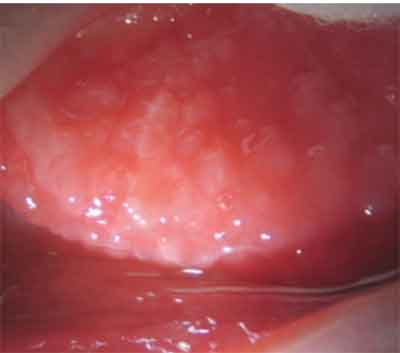
Papillen in GPC sind normalerweise kleiner oder gleich bis 0,3 mm Durchmesser und erscheinen auf der oberen Tarsal-Bindehaut.
Könnte es einen Zusammenhang zwischen der Veranlagung dieser Personen zur Atopie und ihrer Entwicklung der GPC geben? Das Gegenteil ist wahrscheinlich der Fall. Durchbrüche in der Augenoberflächenbarriere von GPC-Patienten erhöhen die Pollenmenge, die zu Mastzellen gelangen kann, was die Wahrscheinlichkeit erhöht, Augenallergien zu entwickeln. Somit können beim Patienten gleichzeitig eine Augenallergie und eine GPC auftreten, was die Diagnose erschwert. Die beiden Zustände können jeweils die Anzeichen und Symptome des anderen verschlimmern und den Gesamtzustand verschlechtern.
Pathophysiologie
Die molekulare Basis der GPC beginnt mit der Störung der normalen Immunabwehr. Dies stimuliert die Produktion und Lokalisierung von Entzündungsmediatoren, einschließlich Neutrophilen, Eosinophilen und Mastzellen, in der Bindehaut.
Die Erforschung der an GPC beteiligten Mediatoren hat mehr Akteure bei den beteiligten Entzündungsprozessen aufgedeckt. In einer kürzlich durchgeführten Studie, in der die Zytokin- und Chemokinprofile von VKC und GPC verglichen wurden, stellten die Forscher einen vier- bzw. achtfachen Anstieg zahlreicher Entzündungsmediatoren bei beiden Erkrankungen fest.4 Die am stärksten erhöhten GPC waren Interleukin-6-lösliche Rezeptoren (IL-6sR). Interleukin-11 (IL-11), Eotaxin-2, Makrophagen-Entzündungsprotein (MIP) -1 Delta und Gewebehemmer von Metalloproteinase-2 (TIMP-2), obwohl im Vergleich nur die Erhöhungen von TIMP-2 und IL-6sR signifikant waren mit Kontrollen. Obwohl einige der gleichen Mediatoren sowohl bei GPC als auch bei VKC erhöht waren, war TIMP-2 der einzige in dieser Studie bewertete Mediator, der bei GPC-Probanden im Vergleich zu denen mit VKC signifikant erhöht war. IL-6sR war sowohl in VKC als auch in GPC signifikant erhöht. Dies, zusammen mit dem Anstieg anderer Zytokine, ihrer Rezeptoren und Chemokine, unterstreicht die Bedeutung dieser Mediatoren für die Pathophysiologie beider Zustände.
Andere Forschungen haben die T-Zell-Profile bei GPC und chronischen Formen von Allergien untersucht, um festzustellen, welche anderen Entzündungsmechanismen neben einer Typ-I-Überempfindlichkeit wirksam sind. Die Verschiebung zu überwiegend Th2-Zytokinen war bei GPC und VKC stärker ausgeprägt, während bei atopischer Keratokonjunktivitis (AKC) ein Th1-ähnliches Zytokinprofil festgestellt wurde.5 Forscher sagen, dass diese Unterschiede die klinischen Manifestationen dieser Zustände erklären und therapeutische Entscheidungen beeinflussen können .
Weitere Untersuchungen ergaben, dass die Entzündungsmarker Humanes Leukozytenantigen (HLA) -DR und interzelluläres Adhäsionsmolekül (ICAM) -1 bei GPC über den Normalwert erhöht waren, obwohl die Erhöhungen geringer waren als bei AKC und VKC.6 von ICAM-1 zeigt wahrscheinlich die Rekrutierung von Leukozyten durch Epithelzellen an.
Die Forscher untersuchten auch eine Reihe von Zytokinen auf ihre Anwesenheit oder Erhöhung in VKC, AKC und GPC. Es wurden einige Unterschiede festgestellt, wie z. B. die Hochregulation des Zytokins RANTES (reguliert bei Aktivierung, normales T exprimiert und sekretiert) in GPC, jedoch nicht in AKC und VKC.6 Die Variabilität des Zytokinprofils bei jeder Krankheit kann potenzielle Ziele für zukünftige Therapien darstellen bei jeder spezifischen Bedingung.
Die Forscher zeigten auch, dass der Hornhautbeteiligung von VKC und AKC eine stärkere Expression von eosinophilen Oberflächenantigenen zugrunde liegt als bei GPC sowie Unterschiede, bei denen Zytokine im Vergleich zu GPC eine herausragende Rolle spielten.7
Die mögliche Beteiligung des Proteins Eotaxin in GPC hat ein gewisses Interesse gewonnen, dies bleibt jedoch umstritten. Einige Untersuchungen zeigen einen erhöhten Eotaxinspiegel in den Tränen von Kontaktlinsenträgern und eine Korrelation zwischen der Schwere der Anzeichen einer GPC und dem Eotaxinspiegel.8 Eine weitere Studie, in der 68 Fälle von GPC aufgrund von Augenprothesen untersucht wurden, ergab keine signifikanten Unterschiede in der Träne Eotaxinspiegel bei diesen Personen im Vergleich zu gesunden Probanden.9 Tatsächlich waren die Eotaxinspiegel bei chronischen GPC verringert. Weitere Untersuchungen könnten feststellen, ob unterschiedliche Ätiologien der GPC tatsächlich zu unterscheidbaren Unterschieden im Profil der exprimierten Entzündungsmediatoren führen oder ob das zeitliche Fortschreiten der GPC von akut zu chronisch den Eotaxinspiegel verändert.
Behandlung
Untersuchungen zur Untersuchung der Mediatoren und der Pathogenese von GPC sowie Vergleiche seiner Ähnlichkeiten und Unterschiede zu chronischen Allergien werden fortgesetzt. Diese Forschung birgt Potenzial für die Entwicklung zukünftiger Therapien.
Das heutige Management von GPC konzentriert sich jedoch am besten auf die Prävention. Das Erkennen und Entfernen der Ursache ist wichtig, um den Zustand zu beheben. Achten Sie bei Kontaktlinsenträgern auf eine konstante Aufmerksamkeit für GPC. Bei linseninduzierten GPC sind weiche Kontaktlinsen häufiger betroffen als harte Linsen.10
Denken Sie daran, dass die Linsenkante die Schlüsselkomponente zur Vorbeugung ist. Wir und andere haben Fälle gesehen, in denen das gleiche Linsenpolymer in beiden Augen verwendet wird, aber jedes einen anderen Linsenrand hat, was zur Entwicklung von GPC nur im höheren kurzsichtigen Auge führt. Solche Fälle veranschaulichen die Assoziation zwischen GPC und Linsenkante, da alle anderen Variablen gesteuert werden.
Darüber hinaus sollte niemand die richtige Hygiene und Tragegewohnheiten der Linsenpflege ablehnen. Studien haben gezeigt, dass die Häufigkeit des Linsenwechsels eng mit der Inzidenz von GPC korreliert. Eine Studie, in der 47 Kontaktlinsenträger untersucht wurden, ergab, dass GPC bei 36% der Probanden auftrat, deren Linsenwechselplan vier Wochen überschritt, gegenüber 4,5% derjenigen, die die Linsen häufiger als einmal alle vier Wochen wechselten.11 Ein häufigerer Linsenwechselplan kann dies jedoch nicht vollständig Die Ergebnisse dieser Studie zeigen, dass dieses Muster des Linsenwechsels dieses Risiko minimieren kann.
Die frühzeitige Identifizierung und Beseitigung des ursächlichen Faktors ist das schnellste Mittel zur Lösung der GPC. Wenn Kontaktlinsen die Ursache sind, reicht eine Entfernung von ein bis drei Wochen normalerweise aus, damit die Symptome nachlassen, obwohl Papillen monatelang verweilen können. Wenn der Verschleiß der Kontaktlinsen wieder auftritt, wechseln Sie den Patienten zu einem anderen Linsentyp, um zu versuchen, ein Linsenkantendesign zu finden, das für diese Person weniger irritierend ist, anstatt dieselbe Linse wieder einzuführen, die zum Zeitpunkt der GPC-Identifizierung verwendet wurde.
Steroide wie Loteprednoletabonat können zur Behandlung von Entzündungen eingesetzt werden, die mit schwereren GPC-Fällen verbunden sind. Dies spricht jedoch nicht die zugrunde liegende Ursache der GPC an, so dass ihre Verwendung gleichzeitig mit einer Unterbrechung des Linsenverschleißes einhergehen sollte und sie nicht langfristig verwendet werden sollten. Mastzellstabilisatoren können ebenfalls verschrieben werden; Da der Mechanismus der GPC jedoch nicht primär ein durch Mastzellen vermittelter Prozess ist, wie dies bei einer saisonalen allergischen Konjunktivitis der Fall ist, sind diese von begrenzter Wirksamkeit.
Wenn wir verstehen, dass eine riesige papilläre Konjunktivitis keine Allergie, sondern eine entzündliche Erkrankung ist, die aus wiederholten mechanischen Reizungen (höchstwahrscheinlich über den Kontaktlinsenrand) resultiert, können wir diese Patienten besser identifizieren und behandeln. Und die Tage der GPC, die sich als echte Allergie tarnt, werden bald vorbei sein.
Dr. Chin ist Assistenzprofessor für Optometrie am New England College of Optometry in Boston. Er praktiziert bei Andover Eye Associates, Andover, Massachusetts, und führt klinische Forschung bei Ophthalmic Research Associates, North Andover, Massachusetts, durch.
1. Greiner JV. Riesige papilläre Bindehautentzündung. In: Allergische Erkrankungen des Auges. Abelson MB, Hrsg. New York: WB Saunders; 2001: 140-60.
3. Begley CG, Riggle A, Tuel JA. Assoziation der riesigen papillären Konjunktivitis mit saisonalen Allergien. Optom Vis Sci 1990; 67: 192.
4. Shoji J., Inada N., Sawa M. Antikörper-Array-erzeugte Zytokinprofile von Tränen von Patienten mit frühlingshafter Keratokonjunktivitis oder riesiger papillärer Konjunktivitis. Jpn J Ophthalmol 2006, Mai-Juni; 50 (3): 195–204.
6. Hingorani M, Calder VL, Buckley RJ, Lightman SL. Die Rolle von Bindehautepithelzellen bei chronischen allergischen Augenerkrankungen. Exp Eye Res 1998 Nov; 67 (5): 491 & ndash; 500.
7. Hingorani M., Calder V., Jolly G. et al. Die Expression von Eosinophilen-Oberflächenantigenen und die Zytokinproduktion variieren bei verschiedenen allergischen Augenerkrankungen. J Allergy Clin Immunol 1998 Nov; 102 (5): 821-30.
9. Sarac O., Erdener U., Irkec M. et al. Tränen-Eotaxinspiegel bei riesiger papillärer Konjunktivitis in Verbindung mit Augenprothesen. Ocul Immunol Inflamm 2003 Sep; 11 (3): 223-30. 10. Donshik PC. Riesige papilläre Konjunktivitis. Trans Am Ophthalmol Soc 1994; 92: 687 & ndash; 744. 11. Donshik PC, Porazinski AD. Riesige papilläre Konjunktivitis bei häufigen Ersatzkontaktlinsenträgern: eine retrospektive Studie. Trans Am Ophthalmol Soc 1999; 97: 205 & ndash; 16.