経験的証拠により、リスク要因、原因、および第一線の介入が明らかになります。
Jeffrey R. Strawn、MD
臨床シンシナティ大学医学部精神科インストラクター
Paul E. Keck Jr、MD
シンシナティ大学医学部精神科教授、社長兼CEO、 Lindner Center of HOPE、シンシナティ、オハイオ州
Stanley N. Caroff、MD
精神医学教授、精神科、ペンシルベニア大学医学部、入院精神医学、精神医学サービス、フィラデルフィアVAメディカルセンター
この生命を脅かす可能性のある症候群はまれであり、その症状はさまざまであるため、神経弛緩性悪性症候群(NMS)の診断と治療については議論の余地があります。これらの要因により、管理された臨床試験で治療を評価することが困難になり、特定の介入の相対的な有効性に関するデータが不足しています。ただし、経験的な臨床データを使用して合理的な治療ガイドラインを作成することは可能かもしれません。1,2
この記事では、NMSの診断と治療の6つの物議を醸す側面に関連する証拠を調べます。
•最も信頼できるリスク要因
•スペクトル障害としてのNMS
•NMSの原因
•第1世代と第2世代の抗精神病薬によって引き起こされるNMS
•一次介入
•NMSエピソード後に抗精神病薬を再開する。
NMSには信頼できるリスク要因がありますか?
小規模な症例管理研究では、抗精神病薬をNMSに服用する患者の素因と考えられる全身的要因として、攪拌、脱水、消耗が最も一貫して見られました(表1).3-5カタトニア症候群と器質性脳症候群は別々のリスク要因である可能性があります。1,6
予備研究でも、遺伝的多型または低血清鉄の影響によって引き起こされるドーパミン受容体の異常が関係しています。1,7、 8薬理学的研究は、より高い用量、迅速な滴定、および抗精神病薬のIM注射はNMSリスクの増加と関連しています。3,5一部の研究では、NMS患者の15%から20%がNMSエピソードの病歴を持っていることが示唆されています1,2。さらに、強力な第1世代抗精神病薬(FGA)—特にハロペリドールは、効力の低い薬や第2世代抗精神病薬(SGA)よりもリスクが高いと考えられていますが、この仮説を証明することは依然として困難です。9-11
ただし、これらのリスク要因はNMSリスクの推定には実用的ではありません。 NMS発生のリスクが低いのに比べて比較的一般的であるため、特定の患者で。精神病症状のある患者の大多数にとって、適切に示された抗精神病薬の薬物療法の利点はリスクを上回ります。
表1NMSのリスクを高めるものは何ですか?
- 攪拌
- 脱水
- 消耗
- 低血清鉄濃度(通常:60〜170 mcg / dL)
診断
- NMSの歴史
- カタトニア
- 有機脳症候群
中枢神経系
- ドーパミン受容体機能障害
- 基底神経節機能障害
- 交感神経系機能障害
薬理学的治療*
- 筋肉内または静脈内注射
- 強力なドーパミン拮抗薬
- 迅速な用量漸増
- 高用量
- SGAと比較したFGA(?)
*個々の患者について、これらの一般的なリスク要因を再度検討する必要があります。抗精神病薬療法の利点
FGA:最初に-世代の抗精神病薬;
SGA:第2世代の抗精神病薬; NMS:神経弛緩性悪性症候群
出典:参考文献1-5
NMSはパーキンソン症候群、緊張病、または悪性高熱症に関連していますか?
パーキンソン症候群。一部の研究者は、NMSを脳内のドーパミン経路の圧倒的な遮断に起因する極端なパーキンソン病の危機として説明しています1,2,12。この見解では、NMSはパーキンソン病患者で突然の中止または喪失後に発生する可能性のあるパーキンソン病-高体温症候群に似ていますドーパミン作動薬を再開することで治療できるドーパミン作動薬療法の有効性13。この見解を裏付ける証拠には、次のものが含まれます。
•パーキンソン病の兆候はNMSの主要な特徴です。 •すべての誘発薬はドーパミン受容体拮抗薬です。
•NMSのリスクは薬のドーパミン受容体親和性と相関します。
•ドーパミン作動薬は効果的な治療法である可能性があります。
•ドーパミン作動性経路の病変は同様の症候群を引き起こします。
•NMSの患者は、ドーパミン代謝物ホモバニル酸の脳脊髄液濃度が低いことを示しています。14
カタトニア。 Fink et al15およびその他16-18は、NMSが薬物誘発性の悪性緊張病の一形態であると説得力を持って主張しています。これを裏付ける証拠は次のとおりです。
•2つの障害は神経精神症状を共有しています。
•緊張病の兆候はNMSで一般的です。19
•悪性緊張病とNMSは生理学的および実験的兆候を共有します。20
•抗精神病薬の再導入は両方の状態を急激に悪化させる可能性があります。
•ベンゾジアゼピンと電気けいれん療法(ECT )は両方の障害の効果的な治療法です。15-18
Lee21は、14人のNMS患者の緊張病の特徴と治療反応との関係を調べました。緊張病症状のあるほとんどの患者はベンゾジアゼピンに反応しましたが、緊張病のない錐体外路温熱症状を示した患者は誰も反応しませんでした。 Leeは、NMSは不均一であり、治療反応が異なる緊張病型と非緊張病型で発生する可能性があると結論付けました。
悪性高熱症。一部の臨床医は、NMSを吸入麻酔薬およびスクシニルコリンによって引き起こされる悪性高熱症と比較しました。1,2証拠には以下が含まれます:
•硬直、高体温、代謝亢進の同様の臨床徴候
•横紋筋融解症などの同様の生理学的および実験的徴候
•ダントロレンに反応する両方の温熱療法。
2つは症状が似ていますが、悪性高熱症は術中に発生し、骨格筋のカルシウム調節の薬理遺伝学的障害を反映しています。さらに、悪性高熱症の硬直は末梢作用性筋弛緩薬に反応しません。1,22証拠は、以前にNMSエピソードを経験した患者が悪性高熱症のリスクがないことを示唆しています。22
病態生理学とはOF NMS?
NMSの病態生理学は複雑であり、複数の中枢および全身経路と神経伝達物質の間の相互作用を伴う可能性があります。上記のように、説得力のある証拠は、ドーパミン遮断が中心的な役割を果たしていることを示唆している12。視床下部におけるドーパミン遮断は、温度調節障害に寄与すると考えられており、黒質線条体系における遮断は、筋肉の硬直および代謝亢進に寄与する可能性が高い。前帯状回-内側眼窩前頭回路および外側眼窩前頭回路へのドーパミン作動性入力の喪失は、NMSで見られる精神状態の変化および緊張病の特徴に寄与する可能性があります。 12
ただし、一部の研究者は、競合する仮説または補完的な仮説を提案しています。たとえば、Gurrera 23は、NMSを発症しやすい患者は、活動亢進および調節不全の交感神経系に対して脆弱であり、この特性は、ドーパミン遮断薬によって誘発されるドーパミン系の破壊とともに、NMSを生成することを提案しました。他の研究者は、セロトニン、ノルエピネフリン、ガンマアミノ酪酸、およびグルタミン作動性メカニズムを示唆しています。 1,12,24,25
FGASまたはSGAがNMSを引き起こす可能性が高いですか?
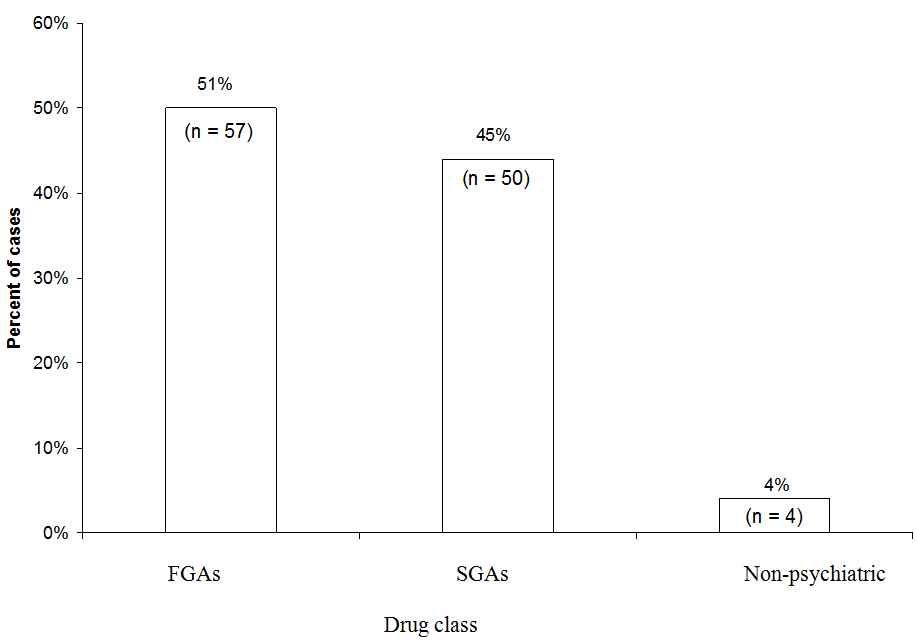
FGA:第1世代の抗精神病薬
SGA:第2世代の抗精神病薬
やや1997年から2006年にNMSホットラインに報告された単一の薬剤に関連する可能性のあるまたは明確なNMSの111症例の分析では、SGA(45%)よりもFGA(51%)に起因するNMS症例が多かった。FGAハロペリドールは44%を占めた。すべての場合の。 「医療」とは、精神病以外の状況で神経弛緩薬が使用された場合を指します。
出典:神経弛緩薬悪性症候群情報サービスに登録されている未発表のデータ。
NMSは、FGAを投与された患者よりも、SGAで治療された患者で発生する頻度が低いと想定されていますが、この仮説は証明されていません。NMSの孤立した報告は、ほぼすべてのSGAに関連付けられています。9-11 FGAとSGAの責任を証明するのが難しい理由は次のとおりです。
•NMSはまれです。
•投薬慣行は以前よりも保守的になっている可能性があります。
•ほとんどの臨床医は、 NMS。
大規模なデータベースの疫学研究で、Stubner et al 26は、SGAを投与された患者はハロペリドールで治療された患者よりもNMSのリスクが低いことを発見しました。26この研究では、NMSの全体的な割合は0.02%。
NMSホットラインデータ。最近、神経遮断薬悪性Sに報告された111のNMS症例にどの薬のクラスが関係しているかを調べました。 1997年から2006年までの症候群情報サービスホットライン(1-888-NMSTEMP)(図)。単一の抗精神病薬が投与された(ホットラインコンサルタントによって診断された)明確なまたは可能性のあるNMSの症例のみを含めました。 SGA(45%)よりもFGA(51%)に起因するケースがわずかに多かった。残りの症例は、医療現場で使用された神経弛緩薬(プロメタジンやプロクロルペラジンなど)に起因していました。
処方頻度が減ったため、FGAはホットラインに報告されたNMS症例の不均衡な数を占めました。ハロペリドールはFGA症例の大部分を占め、全症例の44%を占めました。ハロペリドールを除外し、SGAのNMSリスクを中程度または低効力のFGAのみと比較した場合、SGAの相対的な利点は失われていたでしょう。一方、SGAが依然としてNMSのリスクを抱えていることは明らかです。
分析によると、SGAを投与された患者では、SGAに関連するNMSの古典的な特徴(発熱、筋肉の硬直、自律神経および精神状態の変化)が保持されますが、FGAを投与された患者に一般的な重度の硬直および極端な温度を発症しない場合もあります。 .9-11 SGAに関連するより穏やかな臨床的特徴は、より保守的な処方パターンまたはNMSの認識の向上と早期の認識を反映している可能性があり、これにより、劇症の症状が予防されます。
特定のNMS治療の証拠は何ですか?
NMSはまれであり、その症状はさまざまであり、その進行は予測できません。これらの要因により、管理された臨床試験での治療の評価が困難になり、特定の介入の相対的な有効性に関するデータが不足しています。
それでも、NMSが薬物誘発性パーキンソン症候群または緊張病の極端な変種であるという考えは、特定のNMSが治療は、症状の重症度または症状の段階に基づく可能性があります。理論的メカニズムと事例データに基づいた治療ガイドラインを提案します。2,27-29
サポート。問題のある薬剤を直ちに中止した後、支持療法はNMS治療の基礎となります。1,2,27
軽度の徴候や症状を呈する患者には、支持療法と注意深い臨床モニタリングで十分な場合があります。極度の温熱療法には、大量の蘇生と冷却対策、集中的な医療、合併症の注意深いモニタリングが必要です。
治療。合併症のないNMSの薬物治療に関するコンセンサスが欠如しているにもかかわらず、急性NMS患者の約40%が薬理学的治療を受けています。2
ロラゼパム、1〜2 mgを非経口的に投与することは、NMSの合理的な一次治療です。カタトニックな特徴。4,15-18,21,30,31一部の研究者はより高い用量を推奨しています。15興奮したNMS患者に鎮静が必要な場合はベンゾジアゼピンが好ましいです。4,15-18
ブロモクリプチンやアマンタジンなどのドーパミン作動薬はドーパミン作動性を増強します。パーキンソン病の症状を逆転させるための伝達であり、単独でまたは他の治療法と組み合わせて使用すると、回復までの時間を短縮し、死亡率を半減させることが報告されています。13,27,32,33これらの薬剤の急速な中止は、リバウンド症状を引き起こす可能性がありますが、 NMSの特定の薬物治療に当てはまります。1,31,32
ダントローレンは、骨格筋の筋原形質網状組織におけるカルシウムの隔離を強化することにより、興奮と収縮のカップリングを切り離します。 NMSの代謝亢進症状を治療するために編集されました。一部のレビューでは、ダントロレン単剤療法で治療されたNMS患者の最大80%で改善が見られました。27,32-35ダントロレンを単独でまたは使用した場合、支持療法と比較して、回復までの時間が短縮され、死亡率がほぼ半分に減少する可能性があります。他の薬剤との併用。
すべての症例報告で、ダントロレン、ベンゾジアゼピン、またはドーパミン作動性アゴニストがNMSの治療に有効であることが示されているわけではありません。31,36私たちの意見では、極端な温度上昇、重度の進行したNMS症例のみです。硬直性、および全身性代謝亢進の証拠-ダントロレン治療の恩恵。1,2
ECTは、NMSおよびその他のカタトニックスペクトル障害による死亡率を低下させるために首尾よく使用されています。これは通常、支持療法と精神薬理学的介入が失敗した後に使用されます。2,15,16,27,37急性NMSのECTは通常、両側電極配置による一連の6〜10回の治療で構成されます。最初は毎日のECTが必要になる場合があります。15
NMSエピソードの後に抗精神病薬は禁忌ですか?
抗精神病薬による再治療でのNMSの再発率はさまざまです38。患者の%は、抗精神病薬で再チャレンジしたときにNMS再発のリスクがある可能性があります1。ただし、適切な予防措置に従うことで(表2)、継続的な抗精神病薬療法を必要とするほとんどの患者を安全に治療できます。1,2
治療を再開するとき、限られた利用可能なデータの遡及的分析によれば、異なる化学物質クラスからのより効力の低い抗精神病薬は、誘発剤を再試行するよりも安全な選択肢である可能性があります。 FGAでNMSを発症した患者は、再発のリスクは残っていますが、SGA試験の恩恵を受ける可能性があります。1,10
表2NMSエピソード後の抗精神病薬の再導入
前のNMSエピソードの診断の正確さを再確認する
文書の表示抗精神病薬の場合
再発のリスクを含むリスクとベネフィットについて、患者と家族と話し合います
代替の薬剤を検討します
リスク要因を最小限に抑える(表1)
NMSエピソードが解決した後、再チャレンジする前に2週間以上(長時間作用型の注射薬の場合は4週間以上)許可します
低効力のFGAまたはSGAを選択する
初期試験用量を処方する
生命徴候と神経学的状態を監視する
滴定する徐々に投与する
FGA:第1世代の抗精神病薬;
SGA:第2世代の抗精神病薬
出典:参考文献1,2
関連リソース
•神経遮断薬悪性症候群情報サービス。 www.nmsis.org。
•ZarroufFA、Bhanot V.神経遮断薬悪性症候群:まだ警戒を怠らないでください。 Current Psychiatry 2007; 6(8):89-95。
薬剤のブランド名
アマンタジン•シンメトレル
ブロモクリプチン•パーロデル
クロルプロマジン•ソラジン
ダントロール• Dantrium®
フルフェナジン•プロリキシン
ハロペリドール•ハルドール
ロラゼパム•アチバン
ロキサピン•ロキシタン
ペルフェナジン•トリラフォン
プロクロルペラジン•コンパジン、コンプロ
プロメタジン•フェネルガン
チオリダジン•メラリル
開示
博士Strawnは、アメリカ精神医学会(APIRE)/ JanssenScholarです。
Dr。 Keckは、Abbott Laboratories、American Diabetes Association、AstraZeneca Pharmaceuticals、Bristol-Myers Squibb、GlaxoSmithKline、Eli Lilly and Company、Janssen Pharmaceutica、National Institute of Mental Health、National Institute of Drug Abuse、Pfizerから研究サポートを受けているか、コンサルタントを務めています。 、Stanley Medical Research Institute、およびUCBPharma。
Dr。キャロフは、ブリストルマイヤーズスクイブ、オルソマクニールニューロロジックス、ファイザーから研究支援を受けています。
- キャロフSN。神経遮断薬悪性症候群。In:Mann SC、Caroff SN、Keck PE Jr、Lazarus A、eds。神経遮断薬悪性症候群および関連する状態第2版。ワシントンDC:American Psychiatric Publishing Inc; 2003; 1-44。
- Strawn JR、Keck PE Jr、CaroffSN。神経遮断薬悪性症候群AmJ Psychiatry 2007; 164:870–6。
- Keck PE Jr、Pope HG Jr、Cohen BM、etal。神経遮断薬悪性症候群の危険因子ArchGen Psychiatry 1989; 46:914–18。
- Rosebush PI、StewartTD。神経弛緩薬性悪性症候群の24エピソードの前向き分析AmJ Psychiatry 1989; 146:717–25。
- Berardi D、Amore M、Keck PE Jr、etal。神経弛緩薬性悪性症候群の臨床的および薬理学的危険因子:症例対照研究。 Biol Psychiatry 1998; 44:748–54。
- White DA、RobinsAH。緊張病:神経弛緩薬性悪性症候群の前兆Br J Psychiatry 1991; 158:419–21。
- Rosebush PI、MazurekMF。血清鉄および神経弛緩薬性悪性症候群。 Lancet 1991; 338:149–51。
- LeeJW。緊張病および神経弛緩薬性悪性症候群における血清鉄BiolPsychiatry 1998; 44:499–507。
- Ananth J、Parameswaran S、Gunatilake S、etal。神経遮断薬悪性症候群および非定型抗精神病薬JClin Psychiatry 2004; 65:464–70。
- Caroff SN、Mann SC、CampbellEC。非定型抗精神病薬と神経弛緩薬悪性症候群PsychiatrAnn 2000; 30:314–21。
- Hasan S、BuckleyP。新規抗精神病薬と神経弛緩薬悪性症候群AmJ Psychiatry 1998; 155:1113–16。
- Mann SC、Caroff SN、Fricchione G、Campbell EC中枢ドーパミン活動低下と神経弛緩薬性悪性症候群の病因PsychiatrAnn 2000; 30:363–74。
- ファクターSA、サンティアゴA.パーキンソニズム-パーキンソン病における高呼吸症症候群。 。運動障害の緊急事態:診断と治療。ニュージャージー州トトワ:ヒューマナプレス; 2005; 29-40。
- 西島K、石黒T.神経弛緩薬性悪性症候群におけるモノアミン代謝物とγ-アミノ酪酸の脳脊髄液レベル。 J Psychiatr Res 1995; 27:233–44。
- Fink M、TaylorMA。神経弛緩薬性悪性症候群は悪性緊張病であり、緊張病に有効な治療を保証します。 Prog Neuropsychopharmacol Biol Psychiatry 2006; 30:1182–3。
- Fricchione G、Bush G、Fozdar M、etal。緊張病症候群の認識と治療。 J Intensive Care Med 1997; 12:135–47。
- Philbrick KL、RummansTA。悪性緊張病。 J Neuropsychiatry Clin Neurosci 1994; 6:1–13。
- Mann SC、Caroff SN、Bleier HR、etal。致命的な緊張病。 Am J Psychiatry 1986; 143:1374–81。
- Koch M、Chandragiri S、Rizvi S、etal。神経遮断薬悪性症候群の緊張病の兆候。 Compr Psychiatry 2000; 41:73–5。
- LeeJW。検査結果。で:Caroff SN、Mann SC、Francis A、Fricchoine GL、eds。緊張病:精神病理学から神経生物学までワシントンDC:American Psychiatric Press、Inc; 2004; 65-75。
- リーJW。緊張病性変異、温熱錐体外路反応、および神経弛緩薬性悪性症候群のサブタイプ。 Ann Clin Psychiatry 2007; 19:9–16。
- Caroff SN、Rosenberg H、Mann SC、他。周術期の設定における神経弛緩薬性悪性症候群。 Am J Anesthesiol 2001; 28:387–93。
- GurreraRJ。交感神経副腎機能亢進症と神経弛緩薬性悪性症候群の病因。 Am J Psychiatry 1999; 156:169–80。
- キャロルBT。緊張病および神経弛緩薬性悪性症候群の普遍的なフィールド仮説。 CNS Spectr 2000; 5:26–33。
- Weller M、KornhuberJ。神経弛緩薬性悪性症候群のNMDA受容体拮抗薬療法の理論的根拠。 Med Hypotheses 1992; 38:329–33。
- Stubner S、Rustenbeck E、Grohmann R、etal。向精神薬による重度でまれな不随意運動障害。 Pharmacopsychiatry 2004; 37(suppl 1):S54–S64。
- Davis JM、Caroff SN、MannSC。神経弛緩薬性悪性症候群の治療。 Psychiatr Ann 2000; 30:325–31。
- Adityanjee PA、Singh S、Singh G、OngS。神経弛緩薬性悪性症候群のスペクトル概念。 Br J Psychiatry 1988; 153:107–11。
- Woodbury MM、WoodburyMA。神経弛緩薬性悪性症候群への進行の段階としての神経弛緩薬誘発性緊張病。 J Am Acad Child Adolesc Psychiatry 1992; 31:1161–4。
- Francis A、Chondragivi S、Rizvi S、etal。ロラゼパムは神経弛緩薬性悪性症候群の治療法ですか? CNS Spectr 2000; 5:54–7。
- Rosebush PI、Stewart T、MazurekMF。神経弛緩薬性悪性症候群の治療。ダントロレンとブロモクリプチンは支持療法の補助として有用ですか? Br J Psychiatry 1991; 159:709–12。
- Sakkas P、Davis JM、Janicak PG、WangZY。神経弛緩薬性悪性症候群の薬物治療。 Psychopharmacol Bull 1991; 27:381–4。
- Rosenberg MR、Green M.神経弛緩薬悪性症候群:治療に対する反応のレビュー。 Arch Intern Med 1989; 149:1927–31。
- 山脇S、森尾M、風睦里G他神経弛緩薬性悪性症候群におけるダントロレンナトリウムの臨床評価と効果的な使用法。 Kiso to Rinsyou(Clinical Reports)1993; 27:1045–66。
- ツツミY、ヤマモトK、マツウラS他ダントロレンナトリウムを使用した神経弛緩薬性悪性症候群の治療。 Psychiatry Clin Neurosci 1998; 52:433–8。
- Reulbach U、Dutsch C、Biermann T、etal。神経遮断薬悪性症候群の効果的な治療法の管理。 Crit Care 2007; 11:R4。
- トロラーJN、SachdevPS。神経弛緩薬性悪性症候群の電気けいれん治療:症例のレビューと報告。 Aust N Z J Psychiatry 1999; 33:650–9。
- Pope HG、Aizley HG、Keck PE Jr、McElroySL。神経遮断薬悪性症候群:20例の長期追跡調査。 J Clin Psychiatry 1991; 52:208–12。