La glace flotte car elle est moins dense que leau. Leau a une densité de 1,0 g / cm cube.
La densité de la glace Ih est de 0,931 g / cm cube.
Mais, pourquoi la glace est-elle moins dense que leau si les deux sont fabriquées des molécules de H2O?
————– > spin on ——– > – spin off
—— > space fill / cpk ——– > bâton —- > balle-et-bâton
Pour faire pivoter la molécule — > Clic gauche et glisser
Pour zoomer – > > Clic gauche tout en maintenant la touche Maj enfoncée bouton et faites glisser verticalement
Menu Jsmol — > > Clic droit
Essaye ça!!
Commencez par passer au wireframe:
Cliquez sur le bouton droit de la souris sur la case
Style – > Schémas – – > wireframe
Étiqueter les atomes:
Style – > Étiquette — > numéro atomique
Mesurez les angles suivants:
< 415
< 512
< 213
< 314
Pour mesurer les angles: maintenez le bas gauche de la souris sur latome et double-cliquez sur latome 1, faites glisser vers le deuxième atome (atome central), faites un simple clic sur latome central, faites glisser et double-cliquez sur latome 3.
—— > space fill / cpk ——– > stick —- > balle-et-bâton
Leau liquide a une structure partiellement ordonnée dans laquelle des liaisons hydrogène se forment constamment et se briser.
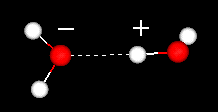
Dautre part, la glace a une structure en treillis rigide.
Dans leau liquide, chaque molécule est liée à lhydrogène à environ 3,4 autres molécules deau.
Dans la glace, chaque molécule est liée à lhydrogène à 4 autres molécules.
Comparez les deux structures ci-dessous. Notez les espaces vides dans la structure de la glace.
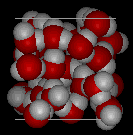 |
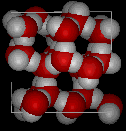 |
Dans la glace Ih, chaque eau se forme quatre liaisons hydrogène avec des distances O — O de 2,76 angströms au voisin oxygène le plus proche. En raison de la structure ordonnée de la glace, il y a moins de molécules H20 dans un espace de volume donné.
Essayez ceci –
Essayez ceci –
1) Mesurez les distances OO entre deux atomes doxygène adjacents dans la glace indiqués dans la structure ci-dessus ..
Veuillez entrer votre réponse dans lespace prévu:
Contrairement à la glace – leau à température ambiante est en mouvement constant – les liaisons hydrogène sont constamment formées et brisées – cliquez ici pour voir les molécules deau en mouvement